
题目列表(包括答案和解析)
【提出猜想】同学们对溶液中Fe3+和![]() 之间的反应进行了猜想,提出了如下观点:
之间的反应进行了猜想,提出了如下观点:
Ⅰ、认为发生相互促进的水解反应,其离子反应方程式为:
2Fe3++3![]() +6H2O
+6H2O![]() 2Fe(OH)3(胶体)+3H2SO3
2Fe(OH)3(胶体)+3H2SO3
Ⅱ、认为发生氧化还原反应,其离子反应方程式为:
2Fe3++![]() +H2O
+H2O![]() 2Fe2++2H++
2Fe2++2H++![]()
【实验验证】为验证“猜想”,同学们实验如下:
(1)取一定量的Na2SO3固体配成Na2SO3浓溶液。
(2)取5 mL FeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,溶液颜色先由黄色变为红棕色,但无气泡产生,无沉淀生成;继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变成红褐色溶液。
(3)换用稀释的FeCl3和Na2SO3溶液重复上述实验,产生的现象完全相同。
(4)为判断红褐色溶液中含有Fe(OH)3从而证明猜想Ⅰ正确。①部分同学认为只要证明该体系为胶体即可,因此通过_____________现象设计实验方案,证明了其为Fe(OH)3胶体;
②部分同学从反证法的角度考虑,认为只要证明红褐色溶液中仍然有+3价的铁,可说明Fe3+没有被还原为Fe2+则猜想Ⅱ不正确,设计方案为,观察到,从而说明红褐色溶液中含有+3价的铁。
(5)另有部分同学认为只要证明红褐色溶液中含有![]() 可判断猜想Ⅱ正确,因此设计方案为_____________,观察到有白色沉淀生成_____________。
可判断猜想Ⅱ正确,因此设计方案为_____________,观察到有白色沉淀生成_____________。
【解释结论】综合(4)(5)考虑,Fe3+与![]() 的反应类型为_____________。
的反应类型为_____________。
【实验反思】某学同认为(5)中![]() 来源不一定是被Fe3+氧化得到的,因此不能推断猜想Ⅱ正确。你是否赞成该同学的观点_____________(填“是”或“否”)。如果赞成,你对实验改进的建议_____________(如果不赞成,该问不必作答)。
来源不一定是被Fe3+氧化得到的,因此不能推断猜想Ⅱ正确。你是否赞成该同学的观点_____________(填“是”或“否”)。如果赞成,你对实验改进的建议_____________(如果不赞成,该问不必作答)。
【拓展探究】鉴于Na2CO3在组成上与Na2SO3相似,某同学在FeCl3溶液中加入Na2CO3溶液,马上观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是_____________;同学们交流后认为二者水溶液与氯化铁溶液反应的现象差别很大,除![]() 有较强的还原性而
有较强的还原性而![]() 没有还原性的原因外,还可能有的原因是__________________________。
没有还原性的原因外,还可能有的原因是__________________________。
下面是某化学学习小组的同学进行探究草酸晶体受热分解的产物和利用其产物进行实验的过程,请你参与并协助他们完成相关学习任务.
[查阅资料]该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:

[提出猜想](1)草酸分解产物中有水;
(2)草酸分解产物中的气体可能是CO、CO2或它们的混合物.
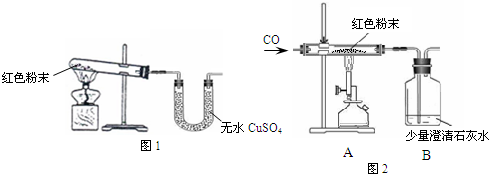
[设计方案]:化学学习小组的同学经过讨论,设计了如下图所示的装置进行“猜想”的实验探究和进行某赤铁矿石经处理后样品的测定.已知:A中装有草酸晶体,B中装有碱石灰,C中装有m g样品(杂质只含有CuO、FeO),D中盛装足量的澄清石灰水.

[讨论与交流]
(1)上图A是用来加热草酸晶体并验证“猜想(1)”的.小华认为该装置错误,正确应是试管口略向下倾斜的,你的判断和理由是______________.
(2)请你设计完成“证明分解产物中有CO2”的实验方案[用简要的实验装置图在方框内表示,要体现所使用仪器和试剂].
(3)证明分解产物中有CO的现象是_______________.
(4)样品在充分还原后,得金属混合物10 g,D中得到20.0 g沉淀.则:
①样品的质量是多少g?;
②通过上述方法制得的金属混合物放置一段时间后,发现表面生锈(铜未生锈),取b g加入1 L 1 mol·L-1的H2SO4溶液中(整个反应过程中无气体产生),完全溶解,最终溶液中c(Fe3+)=0.1 mol·L-1、c(Cu2+)=0.05 mol·L-1,则b的范围是多少(假设反应后溶液的体积为1 L).(写出计算过程)
(5)E装置的作用是_________________.
| ||
| 反应前 | 反应后 | |
| Ⅰ 组 |
玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 |
洗气瓶和所盛溶液 的总质量为180.0g |
洗气瓶和瓶中物质 的总质量为183.1g |
 Fe2O3+3H2O
Fe2O3+3H2O
| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 | 洗气瓶和所盛溶液 的总质量为180.0g | 洗气瓶和瓶中物质 的总质量为183.1g |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com