
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
КЃЫЎЪЧШЫРрзЪдДЕФБІПтЃЌ ЁАКЃЫЎЩЙбЮЁБЪЧЛёШЁЪГбЮЕФживЊРДдДЁЃЪГбЮМШЪЧвЛжжЩњЛюБиашЦЗЃЌвВЪЧвЛжжживЊЕФЙЄвЕдСЯЁЃвдЪГбЮЮЊдСЯПЩвдЕУЕНЖржжВњЦЗЁЃ
ЂХЙЄвЕЩЯгУNaClжЦБИН№ЪєФЦЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦЙЄвЕЩЯжївЊЭЈЙ§ЕчНтБЅКЭТШЛЏФЦШмвКЕФЗНЗЈЛёЕУЧтбѕЛЏФЦЁЃ
ЂйИУЙ§ГЬжавѕМЋЕФВњЮяЪЧЁЁЁЁЁЁЁЁЁЁ ЃЛвѕМЋЗДгІЮЊЃКЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкбєМЋЗДгІЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЃЌМьбщИУЕчМЋЗДгІВњЮяЕФЗНЗЈЪЧЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂлЕБвѕМЋЩЯЪеМЏЕНБъзМзДПіЯТЦјЬх22.4LЪБЃЈМйЩшВњЩњЕФЦјЬхЭъШЋБЛЪеМЏЃЉЃЌдђЕчТЗжаЭЈЙ§ЕчзгЕФЪ§ФПЮЊЁЁЁЁЁЁЁЁЁЁ NAЁЃ
ЂЧЕчНтТШЛЏФЦЯЁШмвКПЩвджЦБИЁА84ЁБЯћЖОвКЃЌШєЭЈЕчЪБВњЩњЕФТШЦјБЛШмвКЭъШЋЮќЪеЃЌЧвзюжеЫљЕУЯћЖОвКНіКЌвЛжжШмжЪЃЌЧыаДГіЯргІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЈгУвЛИіЗНГЬЪНБэЪОЃЉЁЃ
ЂШКЃЫЎЕчНтжЦЕУЕФЧтЦјгУгкКЯГЩАБЃЌФГКЯГЩАБГЇЩњВњСїГЬШчЯТЃК
ЂйдкЕкЃЈ1ЃЉИіЩшБИжаЯШАбN2 ЁЂH2бЙЫѕЕФФПЕФЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂкдкЕкЃЈ3ЃЉИіЩшБИжагУРфШДЕФЗНЗЈЗжРыГіЁЁЁЁЁЁЁЁЁЁ ЦфФПЕФЪЧЃКЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
вРееАЂЗќМгЕТТоЖЈТЩЃЌЯТСаа№Ъіе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(ЁЁ ) A.ЭЌЮТЭЌбЙЯТСНжжЦјЬхЕФЬхЛ§жЎБШЕШгкФІЖћжЪСПжЎБШЁЃ
B.ЭЌЮТЭЌбЙЯТСНжжЦјЬхЕФЮяжЪЕФСПжЎБШЕШгкУмЖШжЎБШЁЃ C.ЭЌЮТЭЌбЙЯТСНжжЦјЬхЕФФІЖћжЪСПжЎБШЕШгкУмЖШжЎБШЁЃD.ЭЌЮТЭЌЬхЛ§ЯТСНжжЦјЬхЕФЮяжЪЕФСПжЎБШЕШгкбЙЧПжЎБШЁЃ
ЩшNAБэЪОАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЁЁЁЁЁЁ ЁЁЃЈ ЁЁЃЉ
A. ДзЫсЕФФІЖћжЪСПгыNAИіДзЫсЗжзгЕФжЪСПдкЪ§жЕЩЯЯрЕШЁЃ
B.БъзМзДПіЯТЃЌвдШЮвтБШЛьКЭЕФЧтЦјКЭвЛбѕЛЏЬМЦјЬхЙВ8.96LЃЌдкзуСПбѕЦјжаГфЗжШМЩеЪБЯћКФбѕЦјЕФЗжзгЪ§ЮЊ0.2 NAЁЃ
C.1L1mol/LCuCl2ШмвКжаКЌгаЕФCu2+ЕФИіЪ§ЮЊNAЁЃ
D.25ЁцЃЌ1.01ЁС105PaЪБЃЌ16gГєбѕЫљКЌЕФдзгЪ§ЮЊNAЁЃЁЁ
ЩшNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФЪ§жЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁ ЁЁЃЈ ЁЁЁЁЃЉ
A.гУЖшадЕчМЋЕчНт500mLБЅКЭЪГбЮЫЎЪБЃЌШєШмвКЕФpHжЕБфЮЊ14ЪБЃЌдђЕчМЋЩЯзЊвЦЕФЕчзгЪ§ФПЮЊNAЁЃ
B.дкБъзМзДПіЯТЃЌИїЮЊ1molЕФЖўбѕЛЏСђЁЂШ§бѕЛЏСђЕФЬхЛ§ОљдМЮЊ22.4LЁЃ
C. дкГЃЮТГЃбЙЯТЃЌ6gЪЏгЂОЇЬхжаЃЌКЌга0.4NAИіЙшбѕЙВМлМќЁЃ
D.120gгЩNaHSO4КЭKHSO3зщГЩЕФЛьКЯЮяжаКЌгаСђдзгNAИіЁЃ
БъзМзДПіЯТЃЌЯТСаЛьКЯЦјЬхЕФЦНОљЪНСППЩФмЪЧ50ЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЃЈ ЁЁЁЁЃЉ
AЃЎСђЛЏЧтКЭЖўбѕЛЏСђЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎвЛбѕЛЏЕЊКЭбѕЦј
CЃЎЖўбѕЛЏСђКЭфхЛЏЧтЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЕтЛЏЧтКЭТШЦј
дквЛИіКуШнУмБеШнЦїжаГфШы11gXЦјЬхЃЈФІЖћжЪСПЮЊ 44gЁЄmol-1ЃЉЃЌбЙЧПЮЊ1ЁС105paЁЃШчЙћБЃГжЮТЖШВЛБфЃЌМЬајГфШыXЦјЬхЃЌЪЙШнЦїФкбЙЧПДяЕН5ЁС105paЁЃдђДЫЪБШнЦїФкЕФЦјЬхXЕФЗжзгЪ§дМЮЊ ЃЈ ЁЁЁЁЃЉ
AЃЎ3.3ЁС1025ЁЁ ЁЁ ЁЁ BЃЎ3.3ЁС1024 CЃЎ7.5ЁС1023ЁЁЁЁ ЁЁ DЃЎ7.5ЁС1022
гЩЖўбѕЛЏЬМЁЂЧтЦјЁЂвЛбѕЛЏЬМзщГЩЕФЛьКЯЦјЬхдкЭЌЮТЁЂЭЌбЙЯТгыЕЊЦјЕФУмЖШЯрЭЌЁЃдђИУЛьКЯЦјЬхжаЖўбѕЛЏЬМЁЂЧтЦјЁЂвЛбѕЛЏЬМЕФЬхЛ§БШЮЊЁЁ ЃЈ ЁЁЁЁЃЉЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
AЃЎ29ЁУ8ЁУ13ЁЁЁЁЁЁ BЃЎ22ЁУ1ЁУ14 CЃЎ13ЁУ8ЁУ29ЁЁ ЁЁ ЁЁ DЃЎ26ЁУ16ЁУ57
ЭЌЮТЁЂЭЌбЙЯТЃЌCO2 КЭNOЕФЛьКЯЦјЬх 20mLЃЌЭЈЙ§зуСПЙ§бѕЛЏФЦКѓЦјЬхЬхЛ§МѕЩйЕН10mLЃЌдђдЛьКЯЦјЬхЕФЬхЛ§БШПЩФмЪЧ ЃЈ ЁЁЁЁЃЉ
AЃЎ1ЁУ1ЁЁЁЁЁЁЁЁ BЃЎ2ЁУ3 CЃЎ3ЁУ2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ1ЁУ4
ввШВКЭввЯЉЕФЛьКЯЦјЬхЭъШЋШМЩеЪБ,ЫљашбѕЦјЕФЬхЛ§ЪЧдЛьКЯЦјЬхЕФ2.7БЖ,дђИУЛьКЯЦјЬхгызуСПЕФH2ЗЂЩњМгГЩЗДгІЪБ,ЯћКФH2ЕФЬхЛ§ЪЧдЛьКЯЦјЬхЬхЛ§ЕФ ЃЈ ЁЁЁЁЃЉЁЁ ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ A.1.6БЖЁЁЁЁЁЁ B.1.8БЖЁЁЁЁЁЁ C.1.4БЖЁЁЁЁЁЁ D.1.2БЖЁЁ
дквЛЖЈЬѕМўЯТ,НЋ5ЬхЛ§NOЁЂ5ЬхЛ§NO2ЁЂ6ЬхЛ§O2ЛьКЯЦјЬхжУгкЪдЙмжа,ВЂНЋЪдЙмЕЙСЂгкЫЎВлжа,ГфЗжЗДгІКѓ,ЪЃгрЦјЬхЕФЬхЛ§ЪЧ ЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ ЃЈ ЁЁЁЁЃЉЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
A.1ЬхЛ§ЁЁЁЁЁЁ B.2ЬхЛ§ЁЁЁЁЁЁ C.3ЬхЛ§ЁЁЁЁЁЁ 4.4ЬхЛ§ЁЁ
19ЪРМЭ,ЛЏбЇМвЖдбѕЛЏяЏЕФЛЏбЇЪНгаељвщ.ОВтЖЈяЏЕФЯрЖддзгжЪСПЮЊ91,ЦфТШЛЏЮяеєЦјЕФУмЖШЪЧЭЌШмЁЂЭЌбЙЯТH2УмЖШЕФ116-117БЖ,ЪдХаЖЯгыТШЛЏЮяМлЬЌЯрЭЌЕФбѕЛЏяЏЕФЛЏбЇЪНЁЁЁЁ ЁЁЁЁ ЃЈ ЁЁЁЁЃЉ
A.ZrOЁЁЁЁЁЁ ЁЁ B.Zr2OЁЁЁЁ ЁЁ ЁЁЁЁC.Zr2O3ЁЁЁЁЁЁ ЁЁD.ZrO2
ГЃЮТЯТЃЌЯђ20LецПеШнЦїжаЭЈШыA molСђЛЏЧтКЭ BmolТШЦјЃЈAЃЌBОљЮЊВЛГЌЙ§5ЕФе§ећЪ§ЃЉЃЌЗДгІЭъШЋКѓЃЌШнЦїФкЦјЬхПЩФмДяЕНЕФзюДѓУмЖШЪЧЁЁЁЁ ЃЈ ЁЁЁЁЃЉ
AЃЎ8.5 gЁЄL-1 ЁЁЁЁ BЃЎ18ЃЎ25gЁЄL-1 CЃЎ18.5 gЁЄL-1ЁЁЁЁЁЁ DЃЎ35.5 gЁЄ L-1
ЃЈ9ЗжЃЉЯТБэБъГіЕФЪЧдЊЫижмЦкБэЕФвЛВПЗждЊЫиЃЌЛиД№ЯТСаЮЪЬтЃК
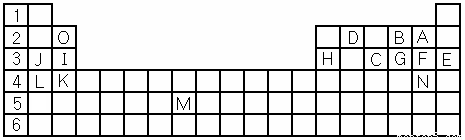
ЃЈ1ЃЉБэжагУзжФИБъГіЕФ15жждЊЫижаЃЌН№ЪєадзюЧПЕФЪЧЁЁ ЃЈгУдЊЫиЗћКХБэЪОЃЌЯТЭЌЃЉЃЌЗЧН№ЪєадзюЧПЕФЪЧ ЃЌГЃЮТЯТЕЅжЪЮЊвКЬЌЕФЗЧН№ЪєдЊЫиЪЧЁЁЁЁ ЃЌЪєгкЙ§ЖЩдЊЫиЕФЪЧ ЁЁЁЁЃЈИУПегУзжФИБэЪОЃЉЁЃ
ЃЈ2ЃЉBЃЌFЃЌCЦјЬЌЧтЛЏЮяжавдЁЁЁЁЁЁЁЁЁЁ зюВЛЮШЖЈЁЃЃЈЬюЛЏбЇЪНЃЉ
ЃЈ3ЃЉГ§ЯЁгаЦјЬхЭтЕкШ§жмЦкжадзгАыОЖзюаЁЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЃЃЈЬюдЊЫиЗћКХЃЉ
ЃЈ4ЃЉаДГіIЁЂHдЊЫиЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсЃЈЛђМюЃЉадЧПШѕЫГађЁЁ ЃОЁЁЁЁ ЃЈгУЛЏбЇЪНБэЪОЃЉ
ЃЈ5ЃЉBЕФЧтЛЏЮяЕчзгЪНЮЊ гУЕчзгЪНБэЪОGЕФЧтЛЏЮяаЮГЩЙ§ГЬ ЃЌЃЈЮяжЪгУЛЏбЇЪНБэЪОЃЉ
ЃЈ9ЗжЃЉЯТБэБъГіЕФЪЧдЊЫижмЦкБэЕФвЛВПЗждЊЫиЃЌЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉБэжагУзжФИБъГіЕФ15жждЊЫижаЃЌН№ЪєадзюЧПЕФЪЧЁЁЃЈгУдЊЫиЗћКХБэЪОЃЌЯТЭЌЃЉЃЌЗЧН№ЪєадзюЧПЕФЪЧ ЃЌГЃЮТЯТЕЅжЪЮЊвКЬЌЕФЗЧН№ЪєдЊЫиЪЧЁЁЁЁЃЌЪєгкЙ§ЖЩдЊЫиЕФЪЧЁЁЁЁЃЈИУПегУзжФИБэЪОЃЉЁЃ
ЃЈ2ЃЉBЃЌFЃЌCЦјЬЌЧтЛЏЮяжавдЁЁЁЁЁЁЁЁЁЁзюВЛЮШЖЈЁЃЃЈЬюЛЏбЇЪНЃЉ
ЃЈ3ЃЉГ§ЯЁгаЦјЬхЭтЕкШ§жмЦкжадзгАыОЖзюаЁЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЃЃЈЬюдЊЫиЗћКХЃЉ
ЃЈ4ЃЉаДГіIЁЂHдЊЫиЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсЃЈЛђМюЃЉадЧПШѕЫГађЁЁ ЃОЁЁЁЁ ЃЈгУЛЏбЇЪНБэЪОЃЉ
ЃЈ5ЃЉBЕФЧтЛЏЮяЕчзгЪНЮЊ гУЕчзгЪНБэЪОGЕФЧтЛЏЮяаЮГЩЙ§ГЬ ЃЌЃЈЮяжЪгУЛЏбЇЪНБэЪОЃЉ
ЃЈ9ЗжЃЉЯТБэБъГіЕФЪЧдЊЫижмЦкБэЕФвЛВПЗждЊЫиЃЌЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉБэжагУзжФИБъГіЕФ15жждЊЫижаЃЌН№ЪєадзюЧПЕФЪЧЁЁ ЃЈгУдЊЫиЗћКХБэЪОЃЌЯТЭЌЃЉЃЌЗЧН№ЪєадзюЧПЕФЪЧ ЃЌГЃЮТЯТЕЅжЪЮЊвКЬЌЕФЗЧН№ЪєдЊЫиЪЧЁЁЁЁ ЃЌЪєгкЙ§ЖЩдЊЫиЕФЪЧ ЁЁЁЁЃЈИУПегУзжФИБэЪОЃЉЁЃ
ЃЈ2ЃЉBЃЌFЃЌCЦјЬЌЧтЛЏЮяжавдЁЁЁЁЁЁЁЁЁЁ зюВЛЮШЖЈЁЃЃЈЬюЛЏбЇЪНЃЉ
ЃЈ3ЃЉГ§ЯЁгаЦјЬхЭтЕкШ§жмЦкжадзгАыОЖзюаЁЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЃЃЈЬюдЊЫиЗћКХЃЉ
ЃЈ4ЃЉаДГіIЁЂHдЊЫиЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсЃЈЛђМюЃЉадЧПШѕЫГађЁЁ ЃОЁЁЁЁ ЃЈгУЛЏбЇЪНБэЪОЃЉ
ЃЈ5ЃЉBЕФЧтЛЏЮяЕчзгЪНЮЊ гУЕчзгЪНБэЪОGЕФЧтЛЏЮяаЮГЩЙ§ГЬ ЃЌЃЈЮяжЪгУЛЏбЇЪНБэЪОЃЉ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com