
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
Đí¶à»¯Ñ§·´Ó¦ÔÚÈÜ̉ºÖĐ½øĐĐ£¬ÏÂĂæµÄÎỀâ¾ùÓëÈÜ̉º»̣ÈÜ̉ºÖеķ´Ó¦ÓĐ¹Ø£®
(1)ijÓêË®ÑùÆ·¸Ơ²É¼¯Ê±²âµĂpHΪ4.82£¬·ÅÔÚÉƠ±ÖĐ¾2Đ¡Ê±ºó£¬ÔٴβâµĂpHΪ4.68£®̉ÔÏÂĐđÊöƠưÈ·µÄÊÇ
[¡¡¡¡]
A£®ÓêË®ÑùÆ·Ëá¶ÈÖđ½¥¼ơĐ¡
B£®ÓêË®ÑùÆ·Ëá¶ÈĂ»ÓĐ±ä»¯
C£®ÓêË®ÑùÆ·¼̀ĐøÎüÊƠ¿ƠÆøÖеÄ
D£®ÓêË®ÑùÆ·ÖеÄ Öđ½¥±»¿ƠÆøÖеÄÑơÆøÑơ»¯³É
Öđ½¥±»¿ƠÆøÖеÄÑơÆøÑơ»¯³É
(2)ÖؽđÊôÀë×ÓÓж¾ĐÔ£®ÊµÑéỂÓĐ¼×¡¢̉̉Á½ÖÖ·Ï̉º£¬¾ùÓĐ̉»¶¨¶¾ĐÔ£®¼×·Ï̉º¾»¯Ñé³Ê¼îĐÔ£¬Ö÷̉ªÓж¾Àë×ÓΪ Àë×Ó£¬È罫¼×¡¢̉̉Á½·Ï̉º°´̉»¶¨±ÈÀư»́ºÏ£¬¶¾ĐÔĂ÷ÏÔ½µµÍ£¬̉̉·Ï̉ºÖĐ¿ÉÄܺ¬ÓеÄÀë×ÓÊÇ
Àë×Ó£¬È罫¼×¡¢̉̉Á½·Ï̉º°´̉»¶¨±ÈÀư»́ºÏ£¬¶¾ĐÔĂ÷ÏÔ½µµÍ£¬̉̉·Ï̉ºÖĐ¿ÉÄܺ¬ÓеÄÀë×ÓÊÇ
[¡¡¡¡]
 ºÍ
ºÍ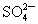
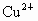 ºÍ
ºÍ
 ºÍ
ºÍ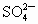
 ºÍ
ºÍ
(3)ijÖÆ̉©³§Î²ÆøÖĐº¬ÉÙÁ¿ Æø̀壬̉»°ăÓĂNaOHÈÜ̉º»̣°±Ë®ÎüÊƠ£¬̉Ô·ÀÎÛȾ»·¾³£®·Ö±đÓĂ0.1mol/LµÄNaOHÈÜ̉º»̣ͬŨ¶ÈµÄ°±Ë®´¦ÀíÏàͬÁ¿µÄβÆø£¬Á½ÖÖ·½·¨ËùĐèÎüÊỞºµÄ̀å»ư¹ØϵÊÇ
Æø̀壬̉»°ăÓĂNaOHÈÜ̉º»̣°±Ë®ÎüÊƠ£¬̉Ô·ÀÎÛȾ»·¾³£®·Ö±đÓĂ0.1mol/LµÄNaOHÈÜ̉º»̣ͬŨ¶ÈµÄ°±Ë®´¦ÀíÏàͬÁ¿µÄβÆø£¬Á½ÖÖ·½·¨ËùĐèÎüÊỞºµÄ̀å»ư¹ØϵÊÇ
[¡¡¡¡]
A£®NaOHÈÜ̉ºµÄ̀å»ư´óÓÚ°±Ë®
B£®NaOHÈÜ̉ºµÄ̀å»ưµÈÓÚ°±Ë®
C£®NaOHÈÜ̉ºµÄ̀å»ưĐ¡ÓÚ°±Ë®
D£®Î̃·¨ÅжÏ
(4)½đÊô¼Ó¹¤ºóµÄ·ÏÇĐÏ÷̉ºÖĐº¬2£¥¡«5£¥µÄ![]() £¬ËüÊÇ̉»ÖÖ»·¾³ÎÛȾÎÈËĂÇÓĂ
£¬ËüÊÇ̉»ÖÖ»·¾³ÎÛȾÎÈËĂÇÓĂ ÈÜ̉ºÀ´´¦Àí´Ë·ÏÇĐÏ÷̉º£¬Ê¹
ÈÜ̉ºÀ´´¦Àí´Ë·ÏÇĐÏ÷̉º£¬Ê¹ ת»¯ÎªÎ̃¶¾ÎïÖÊ£®¸Ă·´Ó¦·ÖÁ½²½½øĐĐ£º
ת»¯ÎªÎ̃¶¾ÎïÖÊ£®¸Ă·´Ó¦·ÖÁ½²½½øĐĐ£º
µÚ̉»²½£º
µÚ¶₫²½£º
ÏÂÁжԵڶ₫²½·´Ó¦µÄĐđÊöÖĐƠưÈ·µÄÊÇ
[¡¡¡¡]
¢Ù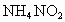 ÊÇÑơ»¯¼Á¡¡¢Ú
ÊÇÑơ»¯¼Á¡¡¢Ú![]() ÊÇ»¹Ô¼Á¡¡¢Û
ÊÇ»¹Ô¼Á¡¡¢Û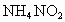 ·¢ÉúÁ˷ֽⷴӦ¡¡¢ÜÖ»ÓеªÔªËصĻ¯ºÏ¼Û·¢ÉúÁ˱仯¡¡¢Ư
·¢ÉúÁ˷ֽⷴӦ¡¡¢ÜÖ»ÓеªÔªËصĻ¯ºÏ¼Û·¢ÉúÁ˱仯¡¡¢Ư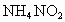 ¼ÈÊÇÑơ»¯¼ÁÓÖÊÇ»¹Ô¼Á
¼ÈÊÇÑơ»¯¼ÁÓÖÊÇ»¹Ô¼Á
Đí¶à»¯Ñ§·´Ó¦ÔÚÈÜ̉ºÖĐ½øĐĐ£¬ÏÂĂæµÄÎỀâ¾ùÓëÈÜ̉º»̣ÈÜ̉ºÖеķ´Ó¦ÓĐ¹Ø£®
(1)ijÓêË®ÑùÆ·¸Ơ²É¼¯Ê±²âµĂpHΪ4.82£¬·ÅÔÚÉƠ±ÖĐ¾2Đ¡Ê±ºó£¬ÔٴβâµĂpHΪ4.68£®̉ÔÏÂĐđÊöƠưÈ·µÄÊÇ
[¡¡¡¡]
A£®ÓêË®ÑùÆ·Ëá¶ÈÖđ½¥¼ơĐ¡
B£®ÓêË®ÑùÆ·Ëá¶ÈĂ»ÓĐ±ä»¯
C£®ÓêË®ÑùÆ·¼̀ĐøÎüÊƠ¿ƠÆøÖеÄ
D£®ÓêË®ÑùÆ·ÖеÄ Öđ½¥±»¿ƠÆøÖеÄÑơÆøÑơ»¯³É
Öđ½¥±»¿ƠÆøÖеÄÑơÆøÑơ»¯³É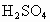
(2)ÖؽđÊôÀë×ÓÓж¾ĐÔ£®ÊµÑéỂÓĐ¼×¡¢̉̉Á½ÖÖ·Ï̉º£¬¾ùÓĐ̉»¶¨¶¾ĐÔ£®¼×·Ï̉º¾»¯Ñé³Ê¼îĐÔ£¬Ö÷̉ªÓж¾Àë×ÓΪ Àë×Ó£¬È罫¼×¡¢̉̉Á½·Ï̉º°´̉»¶¨±ÈÀư»́ºÏ£¬¶¾ĐÔĂ÷ÏÔ½µµÍ£¬̉̉·Ï̉ºÖĐ¿ÉÄܺ¬ÓеÄÀë×ÓÊÇ
Àë×Ó£¬È罫¼×¡¢̉̉Á½·Ï̉º°´̉»¶¨±ÈÀư»́ºÏ£¬¶¾ĐÔĂ÷ÏÔ½µµÍ£¬̉̉·Ï̉ºÖĐ¿ÉÄܺ¬ÓеÄÀë×ÓÊÇ
[¡¡¡¡]
 ºÍ
ºÍ
 ºÍ
ºÍ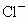
 ºÍ
ºÍ
 ºÍ
ºÍ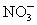
(3)ijÖÆ̉©³§Î²ÆøÖĐº¬ÉÙÁ¿ Æø̀壬̉»°ăÓĂNaOHÈÜ̉º»̣°±Ë®ÎüÊƠ£¬̉Ô·ÀÎÛȾ»·¾³£®·Ö±đÓĂ0.1mol/LµÄNaOHÈÜ̉º»̣ͬŨ¶ÈµÄ°±Ë®´¦ÀíÏàͬÁ¿µÄβÆø£¬Á½ÖÖ·½·¨ËùĐèÎüÊỞºµÄ̀å»ư¹ØϵÊÇ
Æø̀壬̉»°ăÓĂNaOHÈÜ̉º»̣°±Ë®ÎüÊƠ£¬̉Ô·ÀÎÛȾ»·¾³£®·Ö±đÓĂ0.1mol/LµÄNaOHÈÜ̉º»̣ͬŨ¶ÈµÄ°±Ë®´¦ÀíÏàͬÁ¿µÄβÆø£¬Á½ÖÖ·½·¨ËùĐèÎüÊỞºµÄ̀å»ư¹ØϵÊÇ
[¡¡¡¡]
A£®NaOHÈÜ̉ºµÄ̀å»ư´óÓÚ°±Ë®
B£®NaOHÈÜ̉ºµÄ̀å»ưµÈÓÚ°±Ë®
C£®NaOHÈÜ̉ºµÄ̀å»ưĐ¡ÓÚ°±Ë®
D£®Î̃·¨ÅжÏ
(4)½đÊô¼Ó¹¤ºóµÄ·ÏÇĐÏ÷̉ºÖĐº¬2£¥¡«5£¥µÄ![]() £¬ËüÊÇ̉»ÖÖ»·¾³ÎÛȾÎÈËĂÇÓĂ
£¬ËüÊÇ̉»ÖÖ»·¾³ÎÛȾÎÈËĂÇÓĂ ÈÜ̉ºÀ´´¦Àí´Ë·ÏÇĐÏ÷̉º£¬Ê¹
ÈÜ̉ºÀ´´¦Àí´Ë·ÏÇĐÏ÷̉º£¬Ê¹ ת»¯ÎªÎ̃¶¾ÎïÖÊ£®¸Ă·´Ó¦·ÖÁ½²½½øĐĐ£º
ת»¯ÎªÎ̃¶¾ÎïÖÊ£®¸Ă·´Ó¦·ÖÁ½²½½øĐĐ£º
µÚ̉»²½£º
µÚ¶₫²½£º
ÏÂÁжԵڶ₫²½·´Ó¦µÄĐđÊöÖĐƠưÈ·µÄÊÇ
[¡¡¡¡]
¢Ù ÊÇÑơ»¯¼Á¡¡¢Ú
ÊÇÑơ»¯¼Á¡¡¢Ú![]() ÊÇ»¹Ô¼Á¡¡¢Û
ÊÇ»¹Ô¼Á¡¡¢Û ·¢ÉúÁ˷ֽⷴӦ¡¡¢ÜÖ»ÓеªÔªËصĻ¯ºÏ¼Û·¢ÉúÁ˱仯¡¡¢Ư
·¢ÉúÁ˷ֽⷴӦ¡¡¢ÜÖ»ÓеªÔªËصĻ¯ºÏ¼Û·¢ÉúÁ˱仯¡¡¢Ư ¼ÈÊÇÑơ»¯¼ÁÓÖÊÇ»¹Ô¼Á
¼ÈÊÇÑơ»¯¼ÁÓÖÊÇ»¹Ô¼Á
 Ä³Đ£¼×¡¢̉̉¡¢±ûÈư¸ö»¯Ñ§ĐËÈ¤Đ¡×éÀûÓĂ¿ÎÍâ»î¶¯Ê±¼ä£¬Éè¼ÆÁ˲»Í¬µÄ¿Î̀â·Ö±đ½øĐĐÁËʵÑé̀½¾¿»î¶¯£º
Ä³Đ£¼×¡¢̉̉¡¢±ûÈư¸ö»¯Ñ§ĐËÈ¤Đ¡×éÀûÓĂ¿ÎÍâ»î¶¯Ê±¼ä£¬Éè¼ÆÁ˲»Í¬µÄ¿Î̀â·Ö±đ½øĐĐÁËʵÑé̀½¾¿»î¶¯£º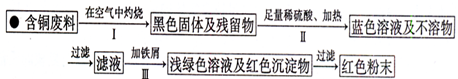

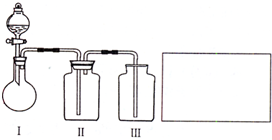
 ijÑĐ¾¿ĐÔÑ§Ï°Đ¡×éΪ֤Ă÷ÔÚͬÎÂͬѹÏ£¬ÏàͬŨ¶ÈÏàͬ̀å»ưµÄ²»Í¬Ç¿¶ÈµÄ̉»ÔªËáÓë×ăÁ¿Ă¾´ø·´Ó¦Ê±£¬Éú³ÉÇâÆøµÄ̀å»ưÏàͬ¶ø·´Ó¦ËÙÂʲ»Í¬£¬Í¬Ê±²â¶¨¸ĂʵÑé̀ơ¼₫ϵÄÆø̀åĦ¶û̀å»ư£¬Éè¼ÆµÄ¼̣̉×ʵÑé×°ÖĂÈçͼ£®¸ĂʵÑéµÄÖ÷̉ª²Ù×÷²½ÖèÈçÏ£º
ijÑĐ¾¿ĐÔÑ§Ï°Đ¡×éΪ֤Ă÷ÔÚͬÎÂͬѹÏ£¬ÏàͬŨ¶ÈÏàͬ̀å»ưµÄ²»Í¬Ç¿¶ÈµÄ̉»ÔªËáÓë×ăÁ¿Ă¾´ø·´Ó¦Ê±£¬Éú³ÉÇâÆøµÄ̀å»ưÏàͬ¶ø·´Ó¦ËÙÂʲ»Í¬£¬Í¬Ê±²â¶¨¸ĂʵÑé̀ơ¼₫ϵÄÆø̀åĦ¶û̀å»ư£¬Éè¼ÆµÄ¼̣̉×ʵÑé×°ÖĂÈçͼ£®¸ĂʵÑéµÄÖ÷̉ª²Ù×÷²½ÖèÈçÏ£º(1)¼×Đ¡×é½øĐĐÖĐºÍµÎ¶¨ÊµÑ飬ʵÑéỂÀï̀ṩÁËÏÂĂ漸ÖÖ̉ÇÆ÷£ºËáʽµÎ¶¨¹Ü¡¢¼îʽµÎ¶¨¹Ü¡¢Á¿Í²¡¢ÍĐÅ̀̀́ƽ¡¢ÆƠͨ©¶·¡¢²£Á§°ô¡¢ÉƠ±£¬ÄăÈÏΪ»¹È±ÉٵIJ£Á§̉ÇÆ÷ÊÇ__________¡£
(2)̉̉Đ¡×éÉè¼ÆÁËÈçÏÂͼËùʾµÄ̉»̀×ʵÑé×°ÖĂ£¬̉Ồ½¾¿¸Ă×°ÖĂµÄ¶à¹¦ÄÜĐÔ¡£

¢ÙÀîĂ÷ͬѧÈÏΪ¸Ă×°ÖĂ¿É̉ÔÓĂÀ´ÖÆÈ¡¡¢ÊƠ¼¯SO2Æø̀壬ÆäÖĐ¢óÖĐÊ¢ÓĐNaOHÈÜ̉º¡£̉̉Đ¡×éͬѧ¾¹ừÖÂÛºóÈÏΪ¸Ă×°ÖĂ´æÔÚ°²È«̉₫»¼£¬Đè̉ª½«¢ó½øĐиÄ×°£¬Ç뽫¸Ä×°ºóµÄ×°ÖĂͼ»ÔÚ·½¿̣ÄÚ¡£
¢ÚÍơǿͬѧÈÏΪ¿ÉÀûÓøĂ×°ÖĂ¿́ËÙÖÆÈ¡¡¢¾»»¯¡¢ÊƠ¼¯°±Æø¡£ÆäÖĐ¢̣ÖĐÊ¢ÓĐŨẠ́Ëá¡£ÄăÈÏΪÊÇ·ñƠưÈ·£¬ÈôƠưÈ·Ộ²»Đè×÷´đ£»Èô²»ƠưÈ·£¬̀á³ö¸Ä½ø̉â¼û___________________¡£
(3)±ûĐ¡×é½øÈëÁË̉»¼̉»ØÊƠº¬ÍµçÀ·ÏÁϵŤ³§×öÉç»áµ÷²é£¬¼¼ÊơÔ±Ị̈ͬѧĂÇƠ¹Ê¾ÁËÁ½¸ö´¦Àí·½°¸£¬²¢Ị̈ͬѧĂÇ̀á³öÏÂÁĐÎỀ⣺
·½°¸1£º

·½°¸2£º

¢ÙÄăÈÏΪ·½°¸___________________¸ü·ûºÏµ±Ç°ẦÉ«Éú²úµÄÀíÄî¡£
¢ÚĐ´³ö·½°¸1ÖĐ²½Öè¢̣·´Ó¦µÄÀë×Ó·½³̀ʽ__________________¡£
¢Û¼¼ÊơÔ±Ö¸³ö£¬Î̃ÂÛÊÇ·½°¸1»¹ÊÇ·½°¸2£¬¶¼Ó¦¼ÓÈëÉÔ¹ưÁ¿µÄ̀úĐ¼²¢×îÖƠ³ưÈ¥£¬ÇëÄăÉè¼Æ³öÈ¥̀úĐ¼µÄ²Ù×÷·½·¨______________________________________________________¡£
¢ÜΪÁËÔö¼Ó¾¼ĂЧ̉棬¸Ă¹¤³§°Ñ×îºó̉»²½ËùµĂdzẦÉ«ÈÜ̉º£¬Í¨¹ư__________________¡¢ÀäÈ´½á¾§¡¢¹ưÂË¡¢Ï´µÓ¡¢×ÔÈ»¸ÉÔïµĂµ½̉»ÖÖË׳ơ°Ầ·¯¡±µÄ¹¤̉µ²úÆ·¡£
¢Ư±û×éͬѧ¾²éѯ×ÊÁÏ¡¢ÑĐ¾¿¡¢̀ÖÂÛ£¬ÓÖÉè¼ÆÁË·½°¸3£¬¼´°Ñ·½°¸2ÖĐ¡°¼ÓÈë×ăÁ¿Ï¡Ạ́ËᡢͨÈë¿ƠÆø²¢¼ÓÈÈ¡±¸ÄΪ¡°¼ÓÈë×ăÁ¿Ï¡Ạ́ËáºÍH2O
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com