
题目列表(包括答案和解析)
(4分 )(1)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101.3 kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH= 436 kJ·mol-1],形成化学键时ΔH<0[如2H(g)=H2(g) ΔH = - 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH = -185 kJ·mol-1
ΔH298(H2)= 436 kJ·mol-1 ,ΔH298(Cl2)= 247 kJ·mol-1
则ΔH298(HCl)= ________________________ 。
(2)已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH = -25 kJ·mol-1
3 Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH = - 47 kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH = 19 kJ·mol-1
请写出CO还原FeO的热化学方程式:________________________________________
(4分 )(1)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101.3 kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH= 436 kJ·mol-1],形成化学键时ΔH<0[如2H(g)=H2(g) ΔH = - 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH = -185kJ·mol-1
ΔH298(H2)= 436 kJ·mol-1 ,ΔH298(Cl2)= 247 kJ·mol-1
则ΔH298(HCl)= ________________________ 。
(2)已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH = -25 kJ·mol-1
3 Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH = - 47kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH = 19 kJ·mol-1
请写出CO还原FeO的热化学方程式:________________________________________
(4分 )(1)化学反应的焓变与反应物和生成物的键能有关。所谓键能就是:在101.3 kPa、298 K时,断开1 mol气态AB为气态A、气态B时过程的焓变,用ΔH298(AB)表示;断开化学键时ΔH>0[如H2(g)=2H(g) ΔH=" 436" kJ·mol-1],形成 化学键时ΔH<0[如2H(g)=H2(g) ΔH =" -" 436 kJ·mol-1]。
化学键时ΔH<0[如2H(g)=H2(g) ΔH =" -" 436 kJ·mol-1]。
已知:H2(g)+Cl2(g)=2HCl(g) ΔH =" -185" kJ·mol-1
ΔH298(H2)=" 436" kJ·mol-1 ,ΔH298(Cl2)=" 247" kJ·mol-1
则ΔH298(HCl)=" ________________________" 。
(2)已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH =" -25" kJ·mol-1
3 Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH =" -" 47 kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH =" 19" kJ·mol-1
请写出CO还原FeO的热化学方程式:________________________________________
(4分)(1)t℃时,测得纯水中c(OH-)=2×10-7mol·L-1, 则t 25℃(填“>”、“<”或“=”),该温度下,水的离子积常数为 ;
(2)25℃时,某K2SO4溶液中c(SO42-)=1×10-4mol·L-1,取该溶液1mL加水稀释至100mL,则稀释后的溶液中c(K+): c(H+)= ;
(3)已知H2(g)+Cl2(g)=2HCl(g) △H=-184.6 kJ/mol;则反应1/2H2(g)+1/2Cl2(g)=HCl(g) 的△H为
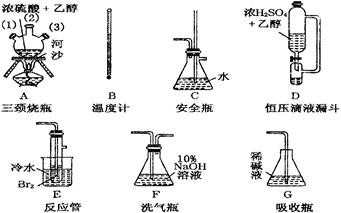
在实验室里用乙醇和浓硫酸反应生成乙烯,再用溴与乙烯反应生成1,2-二溴乙烷,可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。有关数据列表如下:
| | 乙醇 | 1,2二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com