
题目列表(包括答案和解析)
(12分)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 | |
自然界中的硫
认识硫单质
(1)硫的物理性质
硫俗称________,它是一种________色或________色固体,很脆,易研成粉末,________溶于水,________溶于酒精,________溶于CS2;熔点和沸点________.
(2)硫的同素异形体
硫的同素异形体有多种,稳定存在的是斜方硫(S8)和单斜硫(S8).
(3)硫的化学性质
①硫与金属的反应
Fe+S![]()
![]() (Fe有+2、+3价)
(Fe有+2、+3价)
2Cu+S![]()
![]() (Cu有+1、+2价)
(Cu有+1、+2价)
Hg+S![]()
![]() (Hg有+1、+2价)
(Hg有+1、+2价)
②硫与非金属的反应
![]() +O2
+O2![]()
![]() (S是还原剂)
(S是还原剂)
H2+![]()
![]()
![]() (S是氧化剂)
(S是氧化剂)
C+![]()
![]()
![]() (S是氧化剂)
(S是氧化剂)
③黑火药爆炸
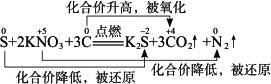
(4)硫的主要用途:制造硫酸、化肥、火柴、杀虫剂、火药、烟花爆竹、医药、硫化橡胶,硫还是酸性速效肥料,等等.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com