
题目列表(包括答案和解析)
| ||
| ||
| ||
| ||
 Al(OH)3+OH-
Al(OH)3+OH- Al(OH)3+OH-
Al(OH)3+OH-

| 3 | 2 |
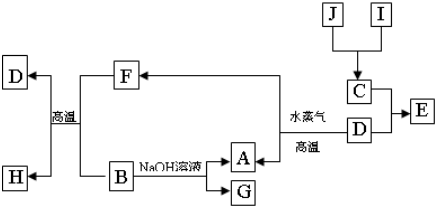
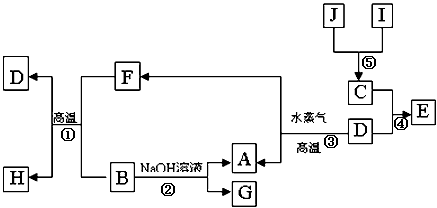
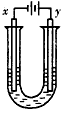
现有五种短周期主族元素A、B、C、 D、E,其原子序数依次增大。A原子约占宇宙中原子总数的88.6%,A+又称为质子:B是形成化合物种类最多的元素,C元素的最简单的氢化物Y的水溶液显碱性.E是短周期元素中电负性最小的元素。A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。试回答下列问题:
(1)写出A、E两元素形成的原子个数比为1:1的化合物的电子式____。
(2)向氯化亚铁溶液滴加过量的E的最高价氧化物对应水化物的溶液,现象是____。
(3)Y溶液显碱性的原因是(用一个离子方程式表示)____。
(4)检验汽车尾气中含有的化合物BD的方法是:向酸性PdC12溶液中通A汽车尾气,若生成黑色沉淀(Pd),证明汽车尾气中含有BD。写出反应的离子方程式____。
(5)下列有关物质性质的比较中.不正确的是 。
a.热稳定性:H2S>SiH4 b.离子半径:Na+>S2-
c.第一电离能N>O d.元素电负性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知.CH3OH的燃烧热____(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的气化热为44 kJ/mol.则表示氢气燃烧热的热化学方程式为____。
一、选择题(30分)
A卷:1.C 2.A 3.D 4.B 5.B
B卷:1.C 2.B 3.D 4.A 5.B
二、非选择题(42分)
30.(共22分)
Ⅰ.(12分)
(1)N是光合酶、ATP、NADP+、叶绿素(叶绿体膜成分)等的组成成分(答案合理即可给分) 倒伏
(2)①a、b ②NH3、CO2 (缺1错1颠倒不给分)
(3)脱氨基 体内缺乏分解或转化三聚氰胺的酶
Ⅱ.(10分)
(1)使胚芽鞘中不含IAA氧化酶(或使原有的IAA氧化酶分解,新的不能合成)
(2)赤霉素可以促进生长素的合成 抑制生长素的分解
(3)伸长生长 两重
31.(20分)
(1)限制性内切酶 DNA聚合酶 四种脱氧核苷酸
(2)B、C(缺1不给分)
(3)植物组织培养
(4)①正反交
②甲×丁或乙×丁
雌性抗除草剂单色耐盐植株 甲或乙
AaXbY


w.w.w.k.s.5.u.c.o.m


w.w.w.k.s.5.u.c.o.m
2009年高三二模化学试题参考答案:
A卷:6.B 7.D 8.B 9.C 10.C 11.A 12.C 13.A
B卷:6.A 7.D 8.D 9.C 10.B 11.A 12.B 13.C
26.(15分)
(1)Cl2 + 2OH- = Cl- + ClO- + H2O(3分)
(2) (2分)
(2分)
(3)Na2CO3 HCl 或NaHCO3 HCl(每空2分,共4分)
(4)C + 2H2SO4(浓)  CO2↑ + 2SO2↑ + 2H2O
CO2↑ + 2SO2↑ + 2H2O
或C + 4HNO3(浓)  CO2↑ + 4NO2↑ + 2H2O (3分)
CO2↑ + 4NO2↑ + 2H2O (3分)
(5)CH3CHO
+ 2Cu(OH)2  CH3COOH + Cu2O + 2H2O(3分)
CH3COOH + Cu2O + 2H2O(3分)
 27.(14分)
27.(14分)
(1) (2分)
(2)2C + SiO2  Si + 2CO↑(3分)
Si + 2CO↑(3分)
(3)Si3N4(2分)
(4)碱性(1分) S2-+H2O HS-+OH-(2分)
HS-+OH-(2分)
(5)金刚石、晶体硅、二氧化硅、甲烷、碳化硅(其他合理答案也可)(4分)
28.(14分)
(1)在分液漏斗中装水,关闭活塞a、b,打开分液漏斗的活塞,过一会儿,若分液漏斗内的水不能顺利流下,同时分液漏斗颈内留有一段水柱,则说明装置A不漏气。(2分)
(2)铁屑逐渐减少,有气泡产生,溶液呈浅绿色;铁与杂质铜形成原电池,加快了反应速率。(每空2分,共4分)
(3)2Fe2+ + 2H+ + H2O2 == 2Fe3+ + 2H2O(3分)
(4)加热蒸干条件下会因Fe3+水解而生成Fe(OH)3(3分)
(5)氯水。(其他合理答案也可)(2分)
29.(17分)
(1)C10H12O2(2分)。
(2) (3分)。
(3分)。
(3)① 取代反应(1分); 加成反应(1分)。
② (2分); 10(2分)。
(2分); 10(2分)。
③ CH2 = CHCH2Cl + NaOH → CH2 = CHCH2OH + NaCl (3分)
 (3分)
(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com