
题目列表(包括答案和解析)
(7分)有人建议根据“最高价阳离子”电子排布的相似性和差异性来分主副族。例如:S、Cr规定为ⅥA族;Se规定为ⅥB族。
1.写出S、Cr、Se最高价阳离子的电子构型;
2.周期数和每周期元素个数是否发生变化;
3.新旧周期表中哪些族的元素是统一的(即完全相同)
4.不同的新的主、副族元素在原周期表的基础上做怎样的变动?
![]()
(1)若A 是一种溶液,其溶质由三种不同短周期元素构成,这三种元素中有两种处于同一主族,且三种元素原子的最外层电子数之和为8,则X的化学式可能为____________、____________(填两种不同类别的物质);若此时X为一种18电子的分子, 则C的化学式为____________,在B的溶液中加入新制的AgCl悬浊液,白色浑浊立即变成黑色浑浊,由此现象可以得出的结论是____________________________________。
(2)若A是一种10电子分子,B在通常情况下遇X即生成C,又知
(3)若A是一种黄色的固体非金属单质,则反应②的化学方程式是_________________。
某温度T时,在一定条件下的
①物质B的转化率____________________________________。
②该温度下反应②的平衡常数____________________________________。
③在上述相同的条件下,向相同的容器中投入2 mol C,请在右下图中画出从反应开始至t2时间达到平衡后各物质的物质的量与时间的关系图。

A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
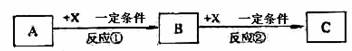
若A是一种溶液,其溶质是由三种不同短周期元素组成,这三种元素原子的最外层电子数之和为8,且有两种元素在周期表中处于同一主族。则X的化学式可能为 、
(填二种不同类别的物质);若X为18电子的分子,则C的化学式是 ,在B溶液中加入新制的AgCl悬浊液,白色浑浊立即变成黑色浑浊,由此现象可以得出的结论是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com