
题目列表(包括答案和解析)
(I) 下图甲和乙是某学校王老师制备NH3 并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL 浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.

将上述中收满NH3 的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O ,此时小气球系在玻璃棒上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3 的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该化学方程式为:__________________________________________________________
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是__________。
①在NH3 · H2O 中有平衡![]() 使平衡向左移动
使平衡向左移动
②在NH3· H2O 中有平衡![]() 使平衡向左移动
使平衡向左移动
③Na0H 溶于水时放热,使体系的温度升高,NH3 的溶解度减小
④NH4Cl与NaOH 在此情况下可反应生成NH3,![]()
⑤NH4Cl 会分解释放出NH3
(3)图甲中的NH4Cl 与NaOH 固体混合物能否用CaO 固体代替 (填”能”与”不能”)
(4)如何判断图甲中烧瓶己收满NH3 ?_____________________________________________
(5)图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是 它说明了NH3

(Ⅱ)如上图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL,则原混合气体中NO2和NO的物质的量之比为
通过导气管C往余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是:
___________________________________________________
有关反应的化学方程式为:___________________________________________
当试管A中充满气体时停止通入氧气,然后将试管取出水槽,则共通入氧气的体积为 ________mL,水槽B中溶液的物质的量浓度为 mol·L-1(设溶液的体积仍为500 mL)
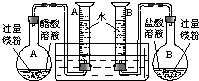 (2009?肇庆二模)某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.
(2009?肇庆二模)某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 |
反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 |
40mL0.1mol/L 盐酸溶液 |
5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
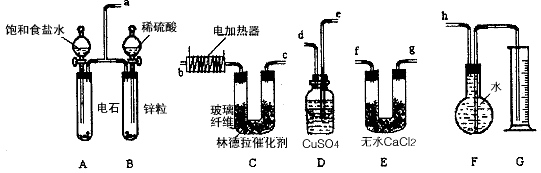
为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如右图所示。回答:
 (1)A装置中反应的化学方程式为
(1)A装置中反应的化学方程式为
(2)B装置的作用是 ;
(3)若省去装置B,C装置中试剂应改为 ,反应的化学方程式为
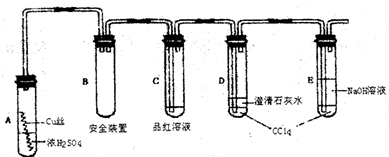
Ⅱ.(10 分)下图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。

填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):___________________________________。
(2)试管C中苯的作用是 ;能说明苯与溴发生的是取代反应而不是加成反应的现象为_______ _____________。
(3)D、E中长导管不插入液面下的原因是 。
(4)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是 。
| ||
| ||
| ||
 Cu(OH)2+2H+
Cu(OH)2+2H+ Cu(OH)2+2H+
Cu(OH)2+2H+湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com