
题目列表(包括答案和解析)
| 催化剂 |
 物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2?2(t-BuNO).在20℃时,向1L正庚烷中加入(t-BuNO)20.50mol,10min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1L).下列说法正确的是( )
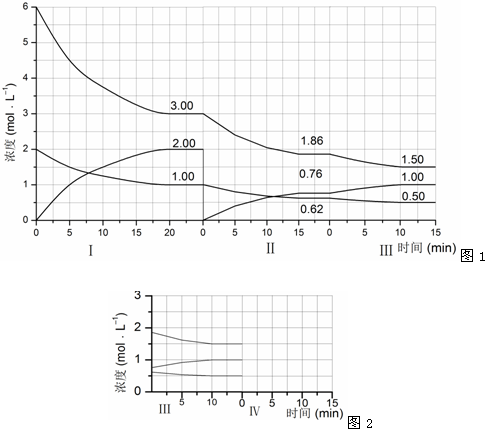
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2?2(t-BuNO).在20℃时,向1L正庚烷中加入(t-BuNO)20.50mol,10min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1L).下列说法正确的是( )反应![]() (△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
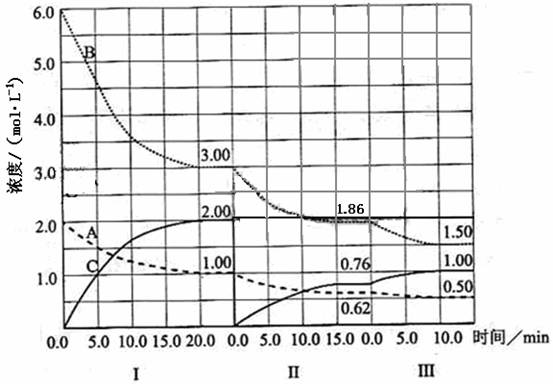 回答问题:
回答问题:
⑴反应的化学方程中a∶b∶c为 ;
 ⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为 ;
⑶B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是 ,其值是 ;
⑷由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
⑸比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2 T3(填“<”“>”“=”)判断的理由是 。
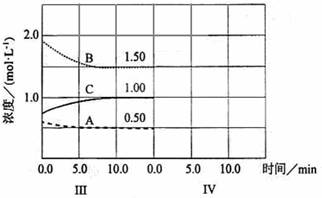
⑹达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示第Ⅳ阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C)。
(1)CD ??????4分,选的不全得2分
(2)①3000;??????3分
② B;?????? 3 分
③ 闭合开关S1,读出电压表的示数U1,再闭合S2,读出电压表的示数U2;
??????4分,少说一个步骤得2分
.files/image075.gif) ??????4分
??????4分
23、参考答案∶16分
H=gt12/2 ??????3分
S1=v0?t1 ??????3分
a=μmg/m ??????3分
v0=at2 因为t2小于t1,所以B先停下。 ??????3分(没有说明的不给这三分)
v02=2as2 ??????3分
△s=s1-s2=
24、参考答案∶ 19分
(1)S=2Rn+R ??????2分
qvB=mv2/R ??????2分
v=.files/image077.gif) ??????2分
??????2分
(2)T=2πR/v=2πm/qB ??????2分
t1=nT/2+T/4 ??????2分
t1=.files/image079.gif) ??????2分
??????2分
在电场中:
a=qE/m ??????2分
v=n at2/2 ??????2分
t2=.files/image081.gif) ??????2分
??????2分
t=t1+t2=.files/image083.gif) 式中n取0、1、2、3 …… 1分 (不说明n不给分)
式中n取0、1、2、3 …… 1分 (不说明n不给分)
25、参考答案∶ 19分
VA=SOP/t ??????2分
vB=4SOP/t ??????2分
.files/image085.gif) ??????4分
??????4分
.files/image087.gif) ??????4分
??????4分
.files/image089.gif)
.files/image091.gif)
vB=-4vA ??????4分
mA:mB=2:3 ??????3分
26.(16分)(1)S H(各1分)(2)N2+3H2 .files/image002.gif) 2NH3 (注意条件) (2分)
2NH3 (注意条件) (2分)
液氨汽化要吸收大量的热(2分) NH3 > H2S(2分)
(3)NH4NO3 (1分) 酸性(1分) NH4++H2O.files/image002.gif) NH3H2O+H+(1分)
NH3H2O+H+(1分)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)(2分) 1014
(4)SO2 (1分) 酸雨(1分)
27.(13分)(1)离子键,非极性键(或共价键)(2分), .files/image093.jpg) (2分)
(2分)
(2)高温、常压、催化剂(2分)
.files/image094.gif) (3)Fe2O3+6H+ 2Fe3++3H2O
(2分)
(3)Fe2O3+6H+ 2Fe3++3H2O
(2分)
.files/image094.gif) Fe2(SO4)3+6NaOH 2Fe(OH)3
↓ +3Na2SO4
(2分)
Fe2(SO4)3+6NaOH 2Fe(OH)3
↓ +3Na2SO4
(2分)
.files/image095.gif) (4)FeS2(s)+
(4)FeS2(s)+.files/image097.gif) O2(g)
O2(g) .files/image099.gif) Fe2O3(s)+2SO2(g);△H=-852kJ/mol (3分)
Fe2O3(s)+2SO2(g);△H=-852kJ/mol (3分)
28.(15分)
.files/image101.jpg)
29.(16分) (1) 棉花团变蓝,刚加热时A中导管有气泡冒出,一会儿停,无浑浊出现,B中持续出现气泡,溶液变白色浑浊 (2分 )
(2) 防止倒吸(或先移出石灰水中导管) 。(2分 )
(3) Na2CO3热稳定性大于NaHCO3 ,NaHCO3受热分解有CO2和H2O生成(2分 )
(4) B 、C (2分 )
|