
题目列表(包括答案和解析)
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示:

焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S === 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。

(3)Al2O3在一定条件下可制得AlN,其晶体结构如右图所示,该晶体中Al
的配位数是 。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,
放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g)![]() 2SO3(g) △H1= -197 kJ /mol;
2SO3(g) △H1= -197 kJ /mol;
H2O(g)![]() H2O(l) △H2=-44 kJ/mol;
H2O(l) △H2=-44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g)===2H2SO4 △H3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是 ① 。
焙烧948 t明矾(M = 474 g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸 ② t。
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示:

焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S = 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图所示,该晶体中Al的配位数是 。

(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g) 2SO3(g)
△H1 = -197 kJ /mol;
2SO3(g)
△H1 = -197 kJ /mol;
H2O(g) H2O(l) △H2 = -44 kJ/mol;
H2O(l) △H2 = -44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g)=2H2SO4(aq) △H3 = -545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是 。
焙烧948 t明矾(M = 474 g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸 t。
明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示: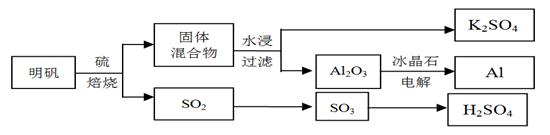
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S = 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图所示,该晶体中Al的配位数是 。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g) 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol;
H2O(g) H2O(l) △H2 = -44 kJ/mol;
H2O(l) △H2 = -44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g)=2H2SO4(aq) △H3 = -545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是 。
焙烧948 t明矾(M =" 474" g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸 t。

 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol; H2O(l) △H2 = -44 kJ/mol;
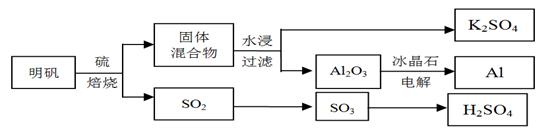
H2O(l) △H2 = -44 kJ/mol;明矾石经处理后得到明矾【 KAl(SO4)2·12H2O】。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O+3S=2K2SO4 +2Al2O3+9SO2+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K2SO4晶体的方法是 。
(3)A12O3在一定条件下可制得AIN,其晶体结构如右图所示,该晶体中Al的配位数是 。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是 。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g) △H1= 一197 kJ/mol;
2SO3(g) △H1= 一197 kJ/mol;
2H2O (g)=2H2O(1) △H2=一44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3=一545 kJ/mol。
则SO3 (g)与H2O(l)反应的热化学方程式是 ① 。
焙烧948t明矾(M=474 g/mol ),若SO2的利用率为96%,可生产质量分数为98%的硫酸 ② t。
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意。)
1.C 2.B 3.B 4.B 5.D 6.D 7.B 8.A 9.B
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确得2分,但只要选错一个就得0分)
10.C 11.C 12.BC 13.D 14.AC 15.AD 16.AB 17.D 18.BD
三、(本题包括3小题,共32分)
19.(10分)
(1)①-----化学.files/image569.gif) [或
[或-----化学.files/image569.gif) 和
和-----化学.files/image572.gif) ](2分)
](2分)
②将-----化学.files/image574.gif) 晶体在干燥的
晶体在干燥的-----化学.files/image194.gif) 气流中加热(1分)
气流中加热(1分)
②关闭-----化学.files/image579.gif) ,打开
,打开-----化学.files/image581.gif) ,通入足量空气后,再打开
,通入足量空气后,再打开-----化学.files/image579.gif) ,关闭
,关闭-----化学.files/image581.gif) (2分)
(2分)
③D中碱石灰会吸收空气中水蒸气和-----化学.files/image078.gif) 等酸性气体,产生误差,测得
等酸性气体,产生误差,测得-----化学.files/image585.gif) 偏大,
偏大,-----化学.files/image587.gif) 偏小(2分)
偏小(2分)
④-----化学.files/image589.gif) (2分)
(2分)
20.(12分)
(2) -----化学.files/image096.gif) (1分) (3)②③(2分)
(1分) (3)②③(2分)
(5)①-----化学.files/image592.gif) (1分)
(1分)
-----化学.files/image594.gif) (血红色)(1分)
(血红色)(1分)
②-----化学.files/image279.gif) 氧化
氧化-----化学.files/image351.gif) ,使平衡
,使平衡-----化学.files/image598.gif)
-----化学.files/image306.gif)
-----化学.files/image600.gif) 左移,红色消失(2分)
左移,红色消失(2分)
③取一支试管,加入少量-----化学.files/image602.gif) 溶液和几滴
溶液和几滴-----化学.files/image604.gif) 溶液,溶液变为红色,再加入适量
溶液,溶液变为红色,再加入适量-----化学.files/image279.gif) 振荡,产生气泡,红色褪去,说明是
振荡,产生气泡,红色褪去,说明是-----化学.files/image279.gif) 氧化了溶液的
氧化了溶液的-----化学.files/image351.gif) 离子使溶液褪色(2分)
离子使溶液褪色(2分)
说明:(1)加入-----化学.files/image279.gif) 与
与-----化学.files/image604.gif) 溶液的顺序可以互换;(2)上面离子方程式的
溶液的顺序可以互换;(2)上面离子方程式的-----化学.files/image351.gif) 写成
写成-----化学.files/image604.gif) 不扣分;(3)简答中要有仪器、试剂、操作、现象、结论共5个要点,现象“产生气泡”和“红色褪去”2点不能少;(4)若把“溶液褪色”答成“溶液变为黄色或棕色”照样给分。
不扣分;(3)简答中要有仪器、试剂、操作、现象、结论共5个要点,现象“产生气泡”和“红色褪去”2点不能少;(4)若把“溶液褪色”答成“溶液变为黄色或棕色”照样给分。
(6)第六步:还原性(1分) -----化学.files/image096.gif) 在人体血红蛋白中起传送
在人体血红蛋白中起传送-----化学.files/image300.gif) 的作用,
的作用,-----化学.files/image357.gif) 没有此功能,服用
没有此功能,服用-----化学.files/image611.gif) 可防止药品的
可防止药品的-----化学.files/image096.gif) 氧化成
氧化成-----化学.files/image357.gif) (或答成人体只能吸收
(或答成人体只能吸收-----化学.files/image096.gif) ,
,-----化学.files/image096.gif) 在人体血红蛋白中起传送
在人体血红蛋白中起传送-----化学.files/image300.gif) 的作用,服用
的作用,服用-----化学.files/image611.gif) 可防止药品的
可防止药品的-----化学.files/image096.gif) 氧化成
氧化成-----化学.files/image357.gif) )(2分)
)(2分)
21.(10分)
(1) -----化学.files/image046.gif) 、
、-----化学.files/image362.gif) (2)
(2) -----化学.files/image046.gif) 、
、-----化学.files/image364.gif) (3)
(3) -----化学.files/image364.gif) 、
、-----化学.files/image362.gif) (每空1分,全对4分,可以互换)
(每空1分,全对4分,可以互换)
(5) -----化学.files/image368.gif) (1分)
(1分) -----化学.files/image572.gif) (1分)
(1分)
(6) -----化学.files/image618.gif)
-----化学.files/image620.gif) (2分)
(2分)
(7)将沉淀A、F洗涤,小心干燥,分别称量(2分)
四、(本题包括3小题,共37分)
22.(共10分)
(1) -----化学.files/image622.gif) (2分)
(2分)
(2) -----化学.files/image624.gif) 、
、-----化学.files/image078.gif) (2分); 不需要(1分)
(2分); 不需要(1分)
(3)22% (2分)
(4) -----化学.files/image627.gif) (1分); 450(2分)
(1分); 450(2分)
23.(15分) w.w.w.k.s.5.u.c.o.m
(1) -----化学.files/image629.gif) (2分)
(2分)
(2)乙(1分) 流程乙中原料-----化学.files/image423.gif) 来源丰富,价格低,工艺流程简单、技术成熟。(2分)
来源丰富,价格低,工艺流程简单、技术成熟。(2分)
(3)①AD(2分)
②经蒸发、浓缩、冷却至
③-----化学.files/image632.gif) (1分) 取出少许滤液置于试管,加稀盐酸至溶液呈酸性后,过滤得出
(1分) 取出少许滤液置于试管,加稀盐酸至溶液呈酸性后,过滤得出-----化学.files/image042.gif) ,再往滤液中加
,再往滤液中加-----化学.files/image106.gif) 溶液,如有白色沉淀即可证明含有
溶液,如有白色沉淀即可证明含有-----化学.files/image632.gif) (2分)
(2分)
④解:若该反应完全得到-----化学.files/image426.gif) :
:
-----化学.files/image638.gif) (1分)
(1分)
若蒸发浓缩得到的-----化学.files/image440.gif) 溶液为饱和溶液,其所含的
溶液为饱和溶液,其所含的-----化学.files/image426.gif) :
:
-----化学.files/image641.gif) (1分)
(1分)
-----化学.files/image643.gif) ,则该溶液尚未饱和,
,则该溶液尚未饱和,
-----化学.files/image645.jpg) 24.(11分)
24.(11分)
(1) -----化学.files/image647.gif) (2分)
(2分)
(2)0.75(2分)
(3)①c;(1分)②参看右图(2分)
(4) -----化学.files/image649.gif) (2分)
(2分)
(5)B、D(2分)
五、(本题包括1小题,9分) w.w.w.k.s.5.u.c.o.m
25.(9分)
(1)AD(2分)
(2)Ⅰ.甲酸钠;氧化反应,取代反应。(3分)
Ⅱ.反应②:-----化学.files/image651.jpg) (2分)
(2分)
反应⑥:-----化学.files/image653.jpg) (2分)
(2分)
六、选做题(本题包括2小题,每小题10分。考生只能选做一题。26小题为“有机化学基础”内容的试题,27小题为“物质结构与性质”内容的试题)
26.(10分)答:
(1)①液体分为两层,上层液体无色,下层液体仍是红棕色;②溴水褪色,产生白色浑浊;③活泼。(每空1分,共3分)
(2)Ⅰ.-----化学.files/image655.gif) (1分)
(1分)
Ⅱ.-----化学.files/image657.jpg) (2分)
(2分)
(3) Ⅰ.-----化学.files/image659.jpg) (2分)
(2分)
Ⅱ.先将-----化学.files/image498.gif) 保护起来,防止酚羟基被
保护起来,防止酚羟基被-----化学.files/image662.gif) 氧化,通过反应⑥再重新生成酚羟基。(1分)
氧化,通过反应⑥再重新生成酚羟基。(1分)
Ⅲ.-----化学.files/image664.gif) 过量,使化学平衡向正反应方向移动;或边反应边蒸馏降低
过量,使化学平衡向正反应方向移动;或边反应边蒸馏降低-----化学.files/image666.gif) 的浓度,使化学平衡向正反应方向移动。(1分)
的浓度,使化学平衡向正反应方向移动。(1分)
27.(10分)
(1) -----化学.files/image668.gif) (1分)
(1分)
(2) -----化学.files/image235.gif) 分子结构为
分子结构为-----化学.files/image671.gif) ,键能大,难断裂生成氮的化合物
,键能大,难断裂生成氮的化合物
-----化学.files/image076.gif) 分子结构为
分子结构为-----化学.files/image674.gif) ,键能小,易断裂生成氯的化合物 (2分)
,键能小,易断裂生成氯的化合物 (2分)
(3) -----化学.files/image519.gif) 分子中的
分子中的-----化学.files/image006.gif) 原子采取
原子采取-----化学.files/image678.gif) 杂化,
杂化,-----化学.files/image537.gif) 分子中的
分子中的-----化学.files/image006.gif) 原子采取
原子采取-----化学.files/image681.gif) 杂化(2分),D(1分)
杂化(2分),D(1分)
(4)6(1分);①离子晶体的晶格能愈大,晶体熔点愈高 ②晶体中离子电荷数愈大,晶格能愈大,熔点愈高 ③晶体中离子间距离愈小,晶格能愈大,熔点愈高(2分,答对2条即可)
(5) -----化学.files/image683.gif) (1分)
(1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com