
题目列表(包括答案和解析)





京京同学对金属活动性顺序等知识进行了研究.
(1)根据下图中的实验现象判断,稀盐酸里的A、B、C、D四种金属中,在金属活动性顺序里,位于氢后面的金属是(填字母)________.

(2)将甲、乙两种金属片分别放入硫酸铜溶液中,乙表面析出红色固体,申没有明显现象.判断甲、乙、铜三种金属的活动性由强到弱的顺序为________.
(3)查阅资料:金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.在下列①②中各写一个化学方程式,③中写出还原金屑氧化物的方法.

(4)查阅资料:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成NO2,NO2是红棕色、有刺激性气味的有毒气体.
用下图所示实验装置进行实验,可以证明铜与稀硝酸反应生成的气体是NO.
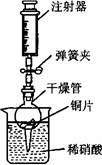
①检查装置的气密性:关闭弹簧夹,将干燥管放人带有水的烧杯中,若观察到________,则表明该装置的气密性良好.
②按上图所示进行实验:打开弹簧夹,用注射器慢慢抽取干燥管内的气体,稀硝酸沿着干燥管慢慢上升,直到________,停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象:________.
反应停止后,打开弹簧夹,用注射器抽取千燥管内的气体(事先已将注射器内原有的气体推出),关闭弹簧夹后取下注射器,并抽取一定量的空气,观察到气体变为红棕色.
③上述实验完成后,用足量NaOH溶液将气体吸收,其目的是________
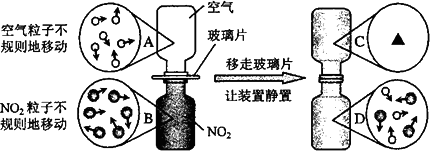
④下图是NO2气体和空气混合的实验示意图,观察图中A、B、D的表示方法,在C处画出相应的气体组成的粒子示意图.
⑤在3.84 g Cu中加入100g稀HNO3溶液,如恰好完全反应,计算生成NO的质量(化学方程式见上)和反应前稀HNO3溶液中溶质的质量分数.(请写出计算过程)


(2008年南京市)京京同学对金属活动性顺序等知识进行了研究。
(1)根据右图中的实验现象判断,稀盐酸里的A、B、C、D
四种金属中,在金属活动性顺序里,位于氢后面的金属是(填 字母) 。
(2)将甲、乙两种金属片分别放入硫酸铜溶液中,乙表面析出红色固体,申没有明显现象。判断甲、乙、铜三种金属的活动性由强到弱的顺序为 。
(3)查阅资料:金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.在下列①②中各写一个化学方程式,③中写出还原金屑氧化物的方法。

(4)查阅资料:在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO ↑ +4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成 N02,N02是红棕色、有刺激性气味的有毒气体。
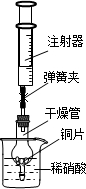
用右下图所示实验装置进行实验,可以证明铜与稀硝酸反应生成的气体是NO。

①检查装置的气密性:关闭弹簧夹,将干燥管放人带有水的烧杯
中,若观察到 ,
则表明该装置的气密性良好。
②按右图所示进行实验:打开弹簧夹,用注射器慢慢抽取干燥管
内的气体,稀硝酸沿着干燥管慢慢上升,直到 ,
停止抽拉注射器,关闭弹簧夹,观察干燥管内的现象:
。
反应停止后,打开弹簧夹,用注射器抽取千燥管内的气体(事先已将注射器内原有的气体推出),关闭弹簧夹后取下注射器,并抽取一定量的空气,观察到气体变为红棕色。
③上述实验完成后,用足量NaOH溶液将气体吸收,其目的是
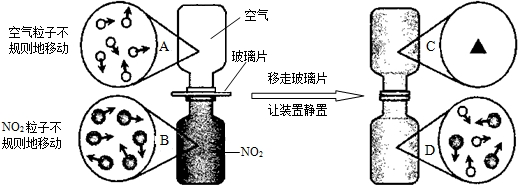
④下图是NO2气体和空气混合的实验示意图,观察图中A、B、D的表示方法,在C处 画出相应的气体组成的粒子示意图。

⑤在3.84 g Cu中加入100 g稀HNO3溶液,如恰好完全反应,计算生成NO的质量
(化学方程式见上)和反应前稀HNO3溶液中溶质的质量分数。 (请写出计算过程)
一、选择题(30分)
1.C 2.A 3.D 4.B 5.B
二、非选择题(42分)
30.(共22分)
Ⅰ.(12分)
(1)N是光合酶、ATP、NADP+、叶绿素(叶绿体膜成分)等的组成成分(答案合理即可给分) 倒伏
(2)①a、b ②NH3、CO2 (缺1错1颠倒不给分)
(3)脱氨基 体内缺乏分解或转化三聚氰胺的酶
Ⅱ.(10分)
(1)使胚芽鞘中不含IAA氧化酶(或使原有的IAA氧化酶分解,新的不能合成)
(2)赤霉素可以促进生长素的合成 抑制生长素的分解
(3)伸长生长 两重
31.(20分)
(1)限制性内切酶 DNA聚合酶 四种脱氧核苷酸
(2)B、C(缺1不给分)
(3)植物组织培养
(4)①正反交
②甲×丁或乙×丁
雌性抗除草剂单色耐盐植株 甲或乙
AaXbY
2009年高三二模化学试题参考答案:
6.B 7.D 8.B 9.C 10.C 11.A 12.C 13.A
26.(15分)
(1)Cl2 + 2OH- = Cl- + ClO- + H2O(3分)
(2) (2分)
(2分)
(3)Na2CO3 HCl 或NaHCO3 HCl(每空2分,共4分)
(4)C + 2H2SO4(浓)  CO2↑ + 2SO2↑ + 2H2O
CO2↑ + 2SO2↑ + 2H2O
或C + 4HNO3(浓)  CO2↑ + 4NO2↑ + 2H2O
(3分)
CO2↑ + 4NO2↑ + 2H2O
(3分)
(5)CH3CHO
+ 2Cu(OH)2  CH3COOH
+ Cu2O + 2H2O(3分)
CH3COOH
+ Cu2O + 2H2O(3分)
 27.(14分)
27.(14分)
(1) (2分)
(2)2C
+ SiO2  Si + 2CO↑(3分)
Si + 2CO↑(3分)
(3)Si3N4(2分)
(4)碱性(1分) S2-+H2O HS-+OH-(2分)
HS-+OH-(2分)
(5)金刚石、晶体硅、二氧化硅、甲烷、碳化硅(其他合理答案也可)(4分)
28.(14分)
(1)在分液漏斗中装水,关闭活塞a、b,打开分液漏斗的活塞,过一会儿,若分液漏斗内的水不能顺利流下,同时分液漏斗颈内留有一段水柱,则说明装置A不漏气。(2分)
(2)铁屑逐渐减少,有气泡产生,溶液呈浅绿色;铁与杂质铜形成原电池,加快了反应速率。(每空2分,共4分)
(3)2Fe2+ + 2H+ + H2O2 == 2Fe3+ + 2H2O(3分)
(4)加热蒸干条件下会因Fe3+水解而生成Fe(OH)3(3分)
(5)氯水。(其他合理答案也可)(2分)
29.(17分)
(1)C10H12O2(2分)。
(2) (3分)。
(3分)。
(3)① 取代反应(1分); 加成反应(1分)。
② (2分); 10(2分)。
(2分); 10(2分)。
③ CH2 = CHCH2Cl + NaOH → CH2 = CHCH2OH + NaCl (3分)
 (3分)
(3分)


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com