
题目列表(包括答案和解析)
NA表示阿伏加德罗常数,下列说法中正确的是
A.3.6 g重氧水(H218O)中所含质子数为2NA
B.4.48 L N2所含分子数为0.2 NA
C.12g金刚石中含有C-C键的个数为2NA
D.1 mol氧气与足量钠点燃反应,转移4NA个电子
NA表示阿伏加德罗常数,下列说法中正确的是( )
A.3.6 g重氧水(H218O)中所含质子数为2NA
B.4.48 L N2所含分子数为0.2 NA
C.12g金刚石中含有C-C键的个数为2NA
D.1 mol氧气与足量钠点燃反应,转移4NA个电子
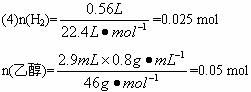
图6-4
(1)若用图6-4中所列仪器和导管组装实验装置,如果所制气体流向从左到右时,仪器和导管连接的顺序是________接________接________接________接________接________。(填编号)
(2)仪器连接好后进行实验时有下列操作:①在仪器C中装入
(3)这样制得的H2中含有什么气体杂质?应该怎样除去?
(4)若实验时消耗2.9 mL无水乙醇(密度为
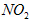 和
和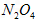 混合气体 4.6 g ,其中含有的原子数为0.3NA ?
混合气体 4.6 g ,其中含有的原子数为0.3NA ? 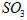 中所含分子数为NA
中所含分子数为NA 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com