研究NO
2、NO、SO
2、CO等大气污染气体的处理具有重要意义。
(1)NO
2可用水吸收,相应的化学反应方程式为____________。利用反应6NO
2(g)+8NH
3(g)

7N
2(g)+12H
2O(g)也可处理NO
2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO
2在标准状况下是_______L。
(2)汽车尾气中含有NO和CO气体,对环境有影响。已知平衡常数K的值大小,是衡量化学反应进行程度的标志。在25℃时,下列反应及平衡常数如下
为了完成汽车尾气处理装置的改造,除去氮氧化物、一氧化碳污染气体,根据上述有关数据判断,下列说法正确的是________
A.改造后的尾气装置使用高温高压,可大量减少污染气体的排放
B.汽车尾气中氮氧化物在空气中会自动的转化为氮肥,对植物生长有益,可不必除去
C.改造后的尾气装置使用催化剂,可大量减少污染气体的排放
D.根据K1和 K2的数据,尾气中NO和CO可自行转化为无害气体
(3)一定条件下将CO和H
2O发生反应,可减少CO对环境的影响。若在700℃时,向容积为2L的密闭容器中充入一定量的CO和H
2O,发生反应:CO(g)+H
2O(g)

CO
2+H
2(g) 反应过程中测定的部分数据见下表(表中t1>t2)
反应在t1min内的平均速率为v(H2)=________ mol·L-1·min-1 保持其他条件不变,起始时向容器中充入2.40molCO和1.20 molH2O,到达平衡时,n(CO2)______0.80 mol(填:大于、小于、等于)。
(4)酸雨是大气污染的危害之一,二氧化硫(SO2)的含量是空气质量监测的一个重要指标。某兴趣小组同学收集某地的雨水进行实验,每隔1h,通过pH计测定雨水样品的pH,测得的结果如下表
请写出上述pH变化的原因(用化学方程式表示)______________________________。

 7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。
7N2(g)+12H2O(g)也可处理NO2。则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是_______L。 
 CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2)
CO2+H2(g) 反应过程中测定的部分数据见下表(表中t1>t2) 

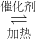 7N2(g)+12H2O(g)也可处理NO2.则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是______L.
7N2(g)+12H2O(g)也可处理NO2.则化学平衡常数表达式K=______;当转移1.2mol电子时,消耗的NO2在标准状况下是______L.
 2C(g);△H<0达到平衡.现只改变下列一个条件时,试依据勒夏特列原理,判断平衡移动的方向.(填向左移动、向右移动、不移动)
2C(g);△H<0达到平衡.现只改变下列一个条件时,试依据勒夏特列原理,判断平衡移动的方向.(填向左移动、向右移动、不移动)