某化学兴趣小组的同学利用课余活动时间,进行有关红磷燃烧的系列实验:
(1)实验一:如图A所示,将点燃的红磷插入充满氧气的集气瓶中,发现红磷剧烈燃烧,产生的现象是:
产生大量的白烟,放出热量,生成一种白色固体
产生大量的白烟,放出热量,生成一种白色固体
,反应的化学方程式为
.

(2)实验二:如图B所示,将过量的红磷点燃后伸入集气瓶中,并立即塞紧瓶塞,待燃烧停止并冷却到原温度后,打开止水夹,观察到的现象是
烧杯中的水倒吸进集气瓶
烧杯中的水倒吸进集气瓶
.瓶内水的体积约点瓶容积的
.该实验的目的是
测定空气中氧气的体积含量
测定空气中氧气的体积含量
(3)若将红磷换成镁带行不行?
行
行
,请说出其中原因之一
生成物都是固体
生成物都是固体
.用化学方程式表示
.若换成铁行不行?
不行
不行
.
(4)实验三:该兴趣小组的同学对如图D、E所示的装置进行探究,原因是
红磷和硫燃烧生成物的状态不同
红磷和硫燃烧生成物的状态不同
,以了解用哪些反应能完成这个实验的目的.
①说出E中产生的现象(燃烧完毕降温到原温度后,打开水止夹)
烧杯内的水不会倒吸进集气瓶
烧杯内的水不会倒吸进集气瓶
.
②你认为
E
E
(D或E)组实验不能达到原实验目的.
(5)实验四,如图C所示,将少量红磷放在一铜片上,用细沙紧密覆盖,用酒精灯在红磷下方加热一段时间,观察不到明显现象,这是因为
红磷没有与氧气接触
红磷没有与氧气接触
.停止加热后,立即除去部分沙子,使红磷暴露在空气中,即看到红磷开始燃烧,这是因为
红磷能与空气接触且温度已经达到了红磷的着火点
红磷能与空气接触且温度已经达到了红磷的着火点
.

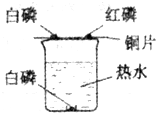 (I)探究燃烧条件的实验装置如下图所示.
(I)探究燃烧条件的实验装置如下图所示.