
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЕчГиЪЧгІгУЙуЗКЕФФмдДЁЃ
ЃЈ1ЃЉЩшМЦСНжжРраЭЕФдЕчГиЃЌБШНЯЦфФмСПзЊЛЏаЇТЪЁЃ
ЯобЁВФСЯЃКZnSO4(aq)ЃЌFeSO4(aq)ЃЌCuSO4(aq)ЃЛЭЦЌЃЌЬњЦЌЃЌаПЦЌКЭЕМЯпЁЃ
ЂйЭъГЩдЕчГиМзЕФзАжУЪОвтЭМЃЈМћгвЭМЃЉЃЌВЂзїЯргІБъзЂЁЃ
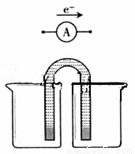
вЊЧѓЃКдкЭЌвЛЩеБжаЃЌЕчМЋгыШмвККЌЯрЭЌЕФН№ЪєдЊЫиЁЃ
ЂквдЭЦЌЮЊЕчМЋжЎвЛЃЌCuSO4(aq)ЮЊЕчНтжЪШмвКЃЌжЛдквЛИіЩеБжазщзАдЕчГиввЁЃ
ЂлМзЁЂввСНжждЕчГижаввЕФФмСПзЊЛЏаЇТЪНЯЕЭЃЌЦфдвђЪЧ ЁЃ
ЃЈ2ЃЉAl-AgOЕчГиПЩзїгУЫЎЯТЖЏСІЕчдДЃЌЦфдРэШчЭМЫљЪОЁЃЦфжаЕФИєФЄЪєгк ЃЈЬюЁАвѕЁБЛђЁАбєЁБЃЉРызгНЛЛЛФЄЁЃИУЕчГиЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК2AlЃЋ3AgOЃЋ2NaOH=2NaAlO2ЃЋ3AgЃЋH2OЃЌаДГіИУЕчГие§ИКМЋЕчМЋЗДгІЃКИКМЋ ЃЌе§МЋ ЁЃ
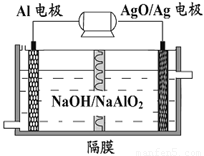
ЛЏбЇЕчГиЪЧ ___ ЕФзАжУЃЌЦфЗДгІЕФЛљДЁЪЧ _ ЁЃаДГіЭаПдЕчГиЃЈЯЁСђЫсЮЊЕчНтжЪЃЉЕФЕчМЋЗДгІЃКе§МЋ ЃЌИКМЋ ЁЃ
ЛЏбЇЕчГиЪЧ ___ ЕФзАжУЃЌЦфЗДгІЕФЛљДЁЪЧ_ ЁЃаДГіЭаПдЕчГиЃЈЯЁСђЫсЮЊЕчНтжЪЃЉЕФЕчМЋЗДгІЃКе§МЋ ЃЌИКМЋ ЁЃ
ЛЏбЇЕчГиЪЧ___ ЕФзАжУЃЌЦфЗДгІЕФЛљДЁЪЧ _ ЁЃаДГіЭаПдЕчГиЃЈЯЁСђЫсЮЊЕчНтжЪЃЉЕФЕчМЋЗДгІЃКе§МЋ ЃЌИКМЋ ЁЃ
ЛЏбЇЪЕбщгажњгкРэНтЛЏбЇжЊЪЖЃЌаЮГЩЛЏбЇЙлФюЃЌЬсИпЬНОПгыДДаТФмСІЃЌЬсЩ§ПЦбЇЫибјЁЃ
ЃЈ1ЃЉдкЪЕбщЪвжагУХЈбЮЫсгыMnO2ЙВШШжЦШЁCl2ВЂНјааЯрЙиЪЕбщЁЃ
ЂйЯТСаЪеМЏCl2ЕФе§ШЗзАжУЪЧ ЁЃ
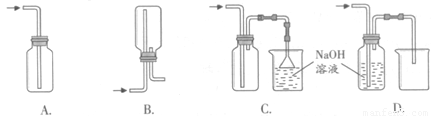
ЂкНЋCl2ЭЈШыЫЎжаЃЌЫљЕУШмвКжаОпгабѕЛЏадЕФКЌТШСЃзгЪЧ ЁЃ
ЂлЩшМЦЪЕбщБШНЯCl2КЭBr2ЕФбѕЛЏадЃЌВйзїгыЯжЯѓЪЧЃКШЁЩйСПаТжЦТШЫЎКЭCCl4гкЪдЙмжаЃЌ ЁЃ
ЃЈ2ЃЉФмСПжЎМфПЩвдЯрЛЅзЊЛЏЃКЕчНтЪГбЮЫЎжЦБИCl2ЪЧНЋЕчФмзЊЛЏЮЊЛЏбЇФмЃЌЖјдЕчГиПЩНЋЛЏбЇФмзЊЛЏЮЊЕчФмЁЃЩшМЦСНжжРраЭЕФдЕчГиЃЌЬНОПЦфФмСПзЊЛЏаЇТЪЁЃ
ЯобЁВФСЯЃКZnSO4(aq)ЃЌFeSO4(aq)ЃЌCuSO4(aq)ЃЛЭЦЌЃЌЬњЦЌЃЌаПЦЌКЭЕМЯпЁЃ
ЂйЭъГЩдЕчГиМзЕФзАжУЪОвтЭМЃЈМћЭМ15ЃЉЃЌВЂзїЯргІБъзЂЁЃ
вЊЧѓЃКдкЭЌвЛЩеБжаЃЌЕчМЋгыШмвККЌЯрЭЌЕФН№ЪєдЊЫиЁЃ
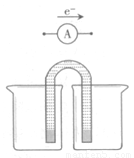
ЂкЭЦЌЮЊЕчМЋжЎвЛЃЌCuSO4(aq)ЮЊЕчНтжЪШмвКЃЌжЛдквЛИіЩеБжазщзАдЕчГиввЃЌЙЄзївЛЖЮЪБМфКѓЃЌПЩЙлВьЕНИКМЋ ЁЃ
ЂлМзввСНжждЕчГижаПЩИќгааЇЕиНЋЛЏбЇФмзЊЛЏЮЊЕчФмЕФЪЧ ЃЌЦфдвђЪЧ ЁЃ
ЃЈ3ЃЉИљОнЮўЩќбєМЋЕФвѕМЋБЃЛЄЗЈдРэЃЌЮЊМѕЛКЕчНтжЪШмвКжаЬњЦЌЕФИЏЪДЃЌдкЃЈ2ЃЉЕФВФСЯжагІбЁ зїбєМЋЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com