
题目列表(包括答案和解析)
甲醇合成反应为:CO(g)+2H2(g) ![]() CH3OH(g) 工业上用天然气为原料,分为两阶段制备甲醇:
CH3OH(g) 工业上用天然气为原料,分为两阶段制备甲醇:
(1)制备合成气:CH4+H2O(g)![]() CO+3H2。为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2:CO2+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧
CO+3H2。为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2:CO2+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧 化碳体积比为__________。
化碳体积比为__________。
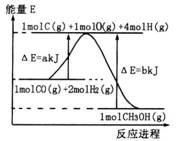
(2)合成甲醇:①反应过程中物质能量变化如右图所示。写出合成甲醇的热化学方程式__________________ 。
实验室在1L密闭容器中进行模拟合成实验。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:
 (表中数据单位:mol·L—1)
(表中数据单位:mol·L—1)
②300℃时反应开始10分钟内,H2的平均反应速率为__________。
③500℃时平衡常数K的数值为___________。
④300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系 产生的影响是__________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
 (3)甲醇直接燃烧会产生一定的污染,某实验小组依据甲醇燃烧的反应原理,设计如图所示甲醇燃料电池, 该电池负极的电极反应式为 ;工作一段时间后,当9.6g甲醇完全反应时,有 NA个电子转移。
(3)甲醇直接燃烧会产生一定的污染,某实验小组依据甲醇燃烧的反应原理,设计如图所示甲醇燃料电池, 该电池负极的电极反应式为 ;工作一段时间后,当9.6g甲醇完全反应时,有 NA个电子转移。
(10分)甲醇合成反应为:CO(g)+2H2(g) CH3OH(g)
工业上用天然气为原料,分为两阶段制备甲醇:
(1)制备合成气:CH4+H2O(g) CO+3H2。为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2:CO3+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为____________________________________。
(2)合成甲醇:①反应过程中物质能量变化如右图所示。写出合成甲醇的热化学方程式__________________。
实验室在1L密闭容器中进行模拟合成实验。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:
(表中数据单位:mol·L—1)
②300℃时反应开始10分钟内,H2的平均反应速率为__________。
③500℃时平衡常数K的数值为___________。
④300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系 产生的影响是__________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
(10分)甲醇合成反应为:CO(g)+2H2(g) 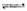 CH3OH(g)
CH3OH(g)
工业上用天然气为原料,分为两阶段制备甲醇:
(1)制备合成气:CH4+H2O(g)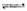 CO+3H2。为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2:CO3+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为____________________________________。
CO+3H2。为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2:CO3+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为____________________________________。
(2)合成甲醇:①反应过程中物质能量变化如右图所示。写出合成甲醇的热化学方程式__________________。
实验室在1L密闭容器中进行模拟合成实验。将lmolCO和2molH2通人容器中,分别恒温在300℃和500℃反应,每隔一定时间测得容器中甲醇的浓度如下:
(表中数据单位:mol·L—1)
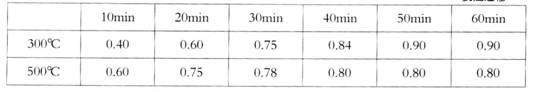 ②300℃时反应开始10分钟内,H2的平均反应速率为__________。
②300℃时反应开始10分钟内,H2的平均反应速率为__________。
③500℃时平衡常数K的数值为___________。
④300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系 产生的影响是__________(填字母)。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时c(H2)/c(CH3OH)减小
KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作如下所示:①称取稍多于所需量的KMnO4固体溶于水中,将溶液加热并保持微沸1 h;②用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;③过滤得到的KMnO4溶液贮存于棕色试剂瓶并放在暗处;④利用氧化还原滴定方法,用基准试剂(纯度高、相对分子质量较大、稳定性较好的物质)溶液标定其浓度,KMnO4在滴定中被还原成Mn2+。请回答下列问题:
(1) 准确量取一定体积的KMnO4溶液需要使用的仪器是____________。
(2) 在下列物质中,用于标定KMnO4溶液的基准试剂最好选用________(填序号)。
A.质量分数为30%的双氧水 B.FeSO4 C.摩尔盐 D.Na2SO3
(3) 本实验也可采用H2C2O4·2H2O做基准试剂,准确称取W g H2C2O4·2H2O溶于水配成500 mL溶液,取25.00 mL置于锥形瓶中,用KMnO4溶液滴定至终点的实验现象为 ,若消耗KMnO4溶液V mL。KMnO4溶液的物质的量浓度为________mol·L-1。
(4) 采用H2C2O4·2H2O做基准试剂的氧化还原滴定在室温时反应很慢,所以反应需要在70~80 ℃条件下进行,但温度更高会导致草酸分解产生气体,写出草酸分解的化学反应方程式 ,若如此所测得的高锰酸钾标准液浓度会 (填“偏高”、“偏低”或“无影响”)。即使控制70~80 ℃条件,一开始滴定时反应仍然较慢,若滴加KMnO4溶液过快的话,会造成KMnO4溶液浓度局部过高而分解,因此在开始几滴操作时应 ,在滴入几滴KMnO4溶液之后,反应速率会迅速加快,该滴定操作也可相应加快,反应速率加快的原因是 。
(5)若用放置两周后的KMnO4标准溶液去测定水样中Fe2+的含量,测得的Fe2+浓度值将________(填“偏高”、“偏低”或“无影响”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com