
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
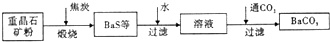
| +CO | 2 3 |
| +SO | 2- 4 |
ЂйH2SO4(aq)+2NaOH(aq) ![]() Na2SO4(aq)+2H2O(l) ЂкH2SO4(aq)+Ba(OH)2(aq)
Na2SO4(aq)+2H2O(l) ЂкH2SO4(aq)+Ba(OH)2(aq) ![]() BaSO4(s)+2H2O(l) ЂлHCl(aq)+NH3ЁЄH2O(aq)
BaSO4(s)+2H2O(l) ЂлHCl(aq)+NH3ЁЄH2O(aq) ![]() NH4Cl(aq)+H2O(l) ЂмCH3COOH(aq)+ NH3ЁЄH2O(aq)
NH4Cl(aq)+H2O(l) ЂмCH3COOH(aq)+ NH3ЁЄH2O(aq) ![]() CH3COONH4(aq)+H2O(l)
CH3COONH4(aq)+H2O(l)
A.ЂйКЭЂк B.Ђл C.Ђм D.вдЩЯЖМВЛЖд
СђдкЕиПЧжажївЊвдСђЛЏЮяЁЂСђЫсбЮЕШаЮЪНДцдкЃЌЦфЕЅжЪКЭЛЏКЯЮядкЙЄХЉвЕЩњВњжагазХживЊЕФгІгУЁЃ
ЃЈ1ЃЉвбжЊЃКжиОЇЪЏЃЈBaSO4ЃЉИпЮТьбЩеПЩЗЂЩњвЛЯЕСаЗДгІЃЌЦфжаВПЗжЗДгІШчЯТЃК
BaSO4(s)+4C(s)=BaS(s)+4CO(g)? ЁїH= + 571.2 kJ?molЁЊ1
BaS(s)= Ba(s)+S(s)? ЁїH= +460 kJ?molЁЊ1
вбжЊЃК2C(s)+O2(g)=2CO(g)? ЁїH= -221 kJ?molЁЊ1
дђЃКBa(s)+S(s)+2O2(g)=BaSO4(s)? ЁїH= ? ? ЁЃ
ЃЈ2ЃЉалЛЦ(As4S4)КЭДЦЛЦ(As2S3)ЪЧЬсШЁЩщЕФжївЊПѓЮядСЯЁЃвбжЊAs2S3КЭHNO3гаШчЯТЗДгІЃК
As2S3+10H++ 10NO3-=2H3AsO4+3S+10NO2Ёќ+ 2H2O
ЕБЗДгІжазЊвЦЕчзгЕФЪ§ФПЮЊ2molЪБЃЌЩњГЩH3AsO4ЕФЮяжЪЕФСПЮЊ?? ЁЃ
ЃЈ3ЃЉЯђЕШЮяжЪЕФСПХЈЖШNa2SЁЂNaOHЛьКЯШмвКжаЕЮМгЯЁбЮЫсжСЙ§СПЁЃЦфжажївЊКЌСђИїЮяжжЃЈH2SЁЂHSЁЊЁЂS2ЁЊЃЉЕФЗжВМЗжЪ§ЃЈЦНКтЪБФГЮяжжЕФХЈЖШеМИїЮяжжХЈЖШжЎКЭЕФЗжЪ§ЃЉгыЕЮМгбЮЫсЬхЛ§ЕФЙиЯЕШчЯТЭМЫљЪОЃЈКіТдЕЮМгЙ§ГЬH2SЦјЬхЕФвнГіЃЉЁЃ
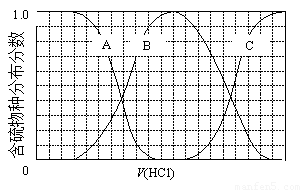
ЂйКЌСђЮяжжBБэЪО???? ЁЃдкЕЮМгбЮЫсЙ§ГЬжаЃЌШмвКжаc(Na+)гыКЌСђИїЮяжжХЈЖШЕФДѓаЁЙиЯЕЮЊ ? (ЬюзжФИ)ЁЃ
aЃЎc(Na+)= c(H2S)+c(HSЁЊ)+2c(S2ЁЊ)
bЃЎ2c(Na+)=c(H2S)+c(HSЁЊ)+c(S2ЁЊ)
cЃЎc(Na+)=3[c(H2S)+c(HSЁЊ)+c(S2ЁЊ)]
ЂкNaHSШмвКГЪМюадЃЌШєЯђШмвКжаМгШыCuSO4ШмвКЃЌЧЁКУЭъШЋЗДгІЃЌЫљЕУШмвКГЪЧПЫсадЃЌЦфдвђЪЧ ? ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃ
ЃЈ4ЃЉСђЕФгаЛњЮяЃЈ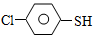 ЃЉгыМзШЉЁЂТШЛЏЧтвдЮяжЪЕФСПжЎБШ1:1:1ЗДгІЃЌПЩЛёЕУвЛжжЩБГцМСжаМфЬхXКЭH2OЁЃ
ЃЉгыМзШЉЁЂТШЛЏЧтвдЮяжЪЕФСПжЎБШ1:1:1ЗДгІЃЌПЩЛёЕУвЛжжЩБГцМСжаМфЬхXКЭH2OЁЃ
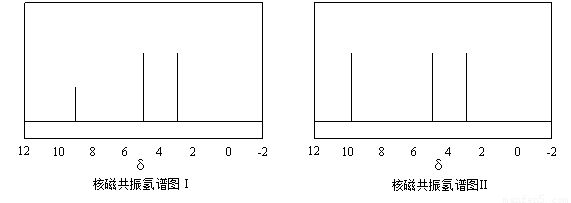
 МАXЕФКЫДХЙВеёЧтЦзШчЯТЭМЃЌЦфжа???? ЃЈЬюЁАЂёЁБЛђЁАЂђЁБЃЉЮЊ
МАXЕФКЫДХЙВеёЧтЦзШчЯТЭМЃЌЦфжа???? ЃЈЬюЁАЂёЁБЛђЁАЂђЁБЃЉЮЊ ЕФКЫДХЙВеёЧтЦзЭМЁЃаДГіXЕФНсЙЙМђЪНЃК???? ЁЃ
ЕФКЫДХЙВеёЧтЦзЭМЁЃаДГіXЕФНсЙЙМђЪНЃК???? ЁЃ
ФГЮТЖШЪБЃЌBaSO4дкЫЎжаЕФГСЕэШмНтЦНКтЧњЯпШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
ЬсЪОЃКBaSO4(s)  Ba2ЃЋ(aq)ЃЋSO(aq)ЕФЦНКтГЃЪ§KSPЃНc(Ba2ЃЋ)ЁЄc(SO )ЃЌГЦЮЊШмЖШЛ§ГЃЪ§ЁЃ
Ba2ЃЋ(aq)ЃЋSO(aq)ЕФЦНКтГЃЪ§KSPЃНc(Ba2ЃЋ)ЁЄc(SO )ЃЌГЦЮЊШмЖШЛ§ГЃЪ§ЁЃ
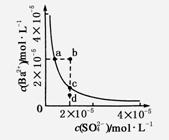
AЃЎМгШыNa2SO4ПЩвдЪЙШмвКгЩaЕуБфЕНbЕу
BЃЎЭЈЙ§еєЗЂПЩвдЪЙШмвКгЩdЕуБфЕНcЕу
CЃЎdЕуЮоBaSO4ГСЕэЩњГЩ
DЃЎaЕуЖдгІЕФKSPДѓгкcЕуЖдгІЕФKSP
25ЁцЃЌ101 kPaЪБЃЌЧПЫсгыЧПМюЕФЯЁШмвКЗЂЩњжаКЭЗДгІЕФжаКЭШШЮЊ57.3 kJ/molЃЌаСЭщЕФШМЩеШШЮЊ5518 kJ/mol.ЯТСаШШЛЏбЇЗНГЬЪНЪщаДе§ШЗЕФЪЧ
AЃЎ2HЃЋ(aq)ЃЋSO42ЁЊ(aq)ЃЋBa2ЃЋ(aq)ЃЋ2OHЃ(aq)===BaSO4(s)ЃЋ2H2O(l)ЃЛІЄHЃНЃ57.3 kJ/mol
BЃЎKOH(aq)ЃЋ1/2H2SO4(aq)===1/2K2SO4(aq)ЃЋH2O(l)ЃЛІЄHЃНЃ57.3 kJ/mol
CЃЎC8H18(l)ЃЋ25/2O2(g)===8CO2(g)ЃЋ9H2O(g)ЃЛІЄHЃНЃ5518 kJ/mol
DЃЎ2C8H18(g)ЃЋ25O2(g)===16CO2(g)ЃЋ18H2O(l)ЃЛІЄHЃНЃ5518 kJ/mol
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com