
题目列表(包括答案和解析)
| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X |  | 0.2 | 45 | 100 |
| Y |  | 1.7 | 114 | 295 |
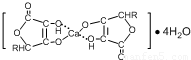
 ④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).
④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).|
物质 |
A级 |
B级 |
|
|
|
|
|
|
NaCl |
KCl |
CsCl |
Na |
Mg |
Al |
|
熔点/K |
1074 |
1049 |
918 |
317 |
923 |
933 |
晶体熔沸点高低,决定于构成晶体粒子间的相互作用的大小.A级是________晶体,晶体粒子之间通过________相连.B组晶体属于________晶体,价电子数由少到多的顺序是________,离子半径由大到小的顺序是________,由库仑定律F=________可知,金属键强度由小到大的顺序为:________________.
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | B、白磷分子晶体中,微粒之间通过共价键结合,键角为60° | C、在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+) | D、离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键不被破坏 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com