
题目列表(包括答案和解析)
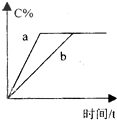 在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+2B(g)?3C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+2B(g)?3C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )| 催化剂 |
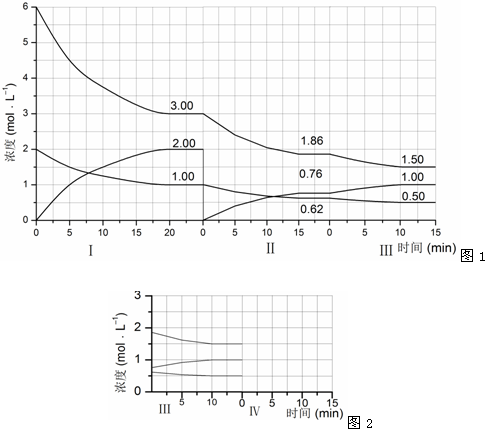
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.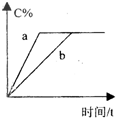 在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)?2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)?2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( ) 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com