
题目列表(包括答案和解析)
(1)下列实验操作或对实验事实的叙述正确的是_____________(填序号)。
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00 mL 0.100 0 mol·L-1 KMnO4溶液;
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸。
(2)为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用图15-15所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试完成下列问题:

图15-15
①指出实验装置中的错误_____________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将_____________(填“偏大”“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)____________。
(05年江苏卷)(10分)请按要求填空:
(1)下列实验操作或对实验事实的叙述正确的是__________________(填序号)
①用稀硝酸清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加到浓硝酸中,并不断搅拌;
③用碱式滴定管量取20.00mL 0.1000mol/L KMnO4溶液;
 ④用托盘天平称取10.50g干燥的NaCl固体;
④用托盘天平称取10.50g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸。
(2)为了确定乙醇分子的结构简式是CH3OCH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题:
①指出实验装置的错误_______________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得氢气的体积将______(填“偏大”、“偏小”或“不变”)。
③请指出能使实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)________________。
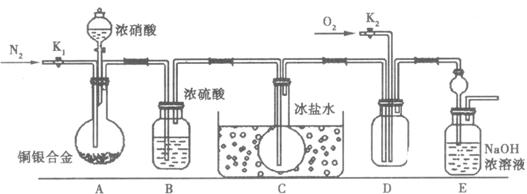
(1)实验开始前先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,其目的是________________________;
(2)装置中B瓶的作用是________________;
(3)A中的反应停止后,打开D中的活塞K2并通入氧气,若反应确有NO产生,则D中应出现的现象是________;实验发现,通入的氧气温度高低对实验现象有较大影响,为便于观察应通入________(填“冷”或“热”)的氧气。
(4)为减小测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是________________________________________________________________。
(5)实验测得下列数据:所用铜银合金质量:15.0 g,浓硝酸:40 mL 13.5 mol/L;实验后A溶液体积:40 mL,H+浓度:1.0 mol/L。假设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为________;②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中铜的质量分数还需测定的数据是________________________________。
(6)已知一定质量的铜银合金粉末,其他试剂和仪器任选,若只要求测定Cu的质量分数,请设计一个简单的实验(只要求写出反映实验原理的化学反应方程式和需要测定的实验数据):________________________________________________________。
为测定镁铝合金(不含其它元素)中铝的质量分数,甲、乙、丙三个学习小组设计了下列三种不同的实验方案进行探究。请回答下列问题:
(一)甲组:实验方案:镁铝合金 测定剩余固体质量
实验步骤:
①称量:托盘天平称量一定质量镁铝合金粉末
②溶解:将①中药品加入烧杯中,加入过量的NaOH溶液,不断搅拌,充分反应。发生反应的离子方程式为
③过滤:
④洗涤:若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变”)
⑤干燥、称量剩余固体
 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金测定生成气体的体积
实验装置如右下图
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个装有碱石灰的干燥装置。你的意见是 (填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(要求写出二点) 、
(三)丙组:实验方案:12 g镁铝合金
操作l包括过滤、洗涤、干燥和称量,并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
为测定镁铝合金(不含其它元素)中铝的质量分数,甲、乙、丙三个学习小组设计了下列三种不同的实验方案进行探究。请回答下列问题: (一)甲组:实验方案:镁铝合金
(一)甲组:实验方案:镁铝合金 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称量:托 盘天平称量一定质量镁铝合金粉末
盘天平称量一定质量镁铝合金粉末
②溶解:将①中药品加入烧杯中,加入过量的NaOH溶液,不断搅拌,充分反应。发生反应的离子方程式为
③过滤:
④洗涤:若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变”)
⑤干燥、称量剩余固体 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积
实验装置如右下图
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个装有碱石灰的干燥装置。你的意见是 (填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(要求写出二点) 、
(三)丙组:实验方案:12 g镁铝合金
操作l包括过滤、洗涤、干燥和称量, 并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com