£Ø2011?ŗž±±Ä£Äā£©X”¢Y”¢Z”¢M”¢N”¢KŹĒÓɶĢÖÜĘŚŌŖĖŲ¹¹³ÉµÄĪ¢Į££¬ĘäÖŠX”¢Y”¢ZŹĒŃōĄė×Ó£¬M”¢NŹĒÖŠŠŌ·Ö×Ó£¬KŹĒŅõĄė×Ó£¬ĖüĆĒ¾ßÓŠĻĀĮŠ½į¹¹ĢŲµćŗĶŠŌÖŹ£ŗ
¢ŁĖüĆĒŗĖĶāµē×Ó×ÜŹż¶¼ĻąĶ¬£»
¢ŚNČÜÓŚMÖŠ£¬µĪČė·ÓĢŖ£¬ČÜŅŗ±äŗģ£»
¢ŪXŗĶN¶¼ÓÉA”¢CĮ½ŌŖĖŲ×é³É£¬XŗĶYŗĖÄŚÖŹ×ÓŹżĻąµČ£»
¢ÜYŗĶK¶¼ÓÉA”¢BĮ½ŌŖĖŲ×é³É£¬YŗĖÄŚÖŹ×Ó×ÜŹż±ČK¶ąĮ½øö£»
¢ŻZĪŖµ„ŗĖĄė×Ó£¬ĒŅĄė×Ó°ė¾¶ŹĒÓėĘä¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹Ąė×ÓÖŠ°ė¾¶×īŠ”µÄ£®
øł¾ŻŅŌÉĻŠÅĻ¢£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©YµÄ»ÆѧŹ½ĪŖ
H3O+
H3O+
£¬XµÄµē×ÓŹ½ĪŖ
£®
£Ø2£©ŹŌ±Č½ĻMŗĶNµÄĪČ¶ØŠŌ£ŗM
£¾
£¾
N£ØĢī”°£¾”±”¢”°£¼”±”¢”°=”±£©
£Ø3£©¼ģŃéXµÄ·½·ØŹĒ
ÓĆŹŌ¹ÜČ”ŗ¬XµÄČÜŅŗÉŁĮ棬¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬¼ÓČČ£¬²śÉśÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢå
ÓĆŹŌ¹ÜČ”ŗ¬XµÄČÜŅŗÉŁĮ棬¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ£¬¼ÓČČ£¬²śÉśÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢå
£®
£Ø4£©ÓÉA”¢B”¢CČżÖÖŌŖĖŲ×é³ÉµÄĪļÖŹÖŠ£¬ŹōÓŚĄė×Ó»ÆŗĻĪļµÄÓŠ
NH4NO3µČ
NH4NO3µČ
£¬ŹōÓŚ¹²¼Ū»ÆŗĻĪļµÄÓŠ
HNO3µČ
HNO3µČ
£Øø÷ČĪŠ“Ņ»ÖÖĪļÖŹµÄ»ÆѧŹ½£©
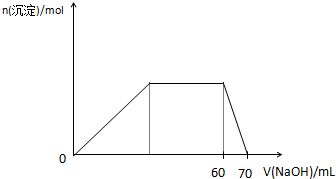
£Ø5£©ÉĻŹöĮłÖÖĪ¢Į£ÖŠµÄĮ½ÖÖæÉÓėĮņĖįøłŠĪ³ÉŅ»ÖÖø“ŃĪ£¬ĻņøĆŃĪµÄÅØČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/LĒāŃõ»ÆÄĘČÜŅŗ£¬Ėę×ÅĒāŃõ»ÆÄĘČÜŅŗµÄ¼ÓČė£¬²śÉś³ĮµķµÄ¹ŲĻµČēĶ¼£¬ŌņøĆø“ŃĪµÄ»ÆѧŹ½ĪŖ
£ØNH4£©3Al£ØSO4£©3»ņ3£ØNH4£©2SO4©qAl2£ØSO4£©3
£ØNH4£©3Al£ØSO4£©3»ņ3£ØNH4£©2SO4©qAl2£ØSO4£©3
£®

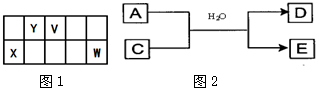


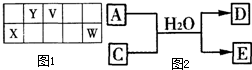 V”¢W”¢X”¢Y”¢ZŹĒĪåÖÖ³£¼ūŌŖĖŲ£¬ĘäÖŠV”¢W”¢X”¢YĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼1Ź¾£ŗV”¢WµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļM”¢N»ģŗĻŹ±ÓŠ°×ŃĢÉś³É£¬MÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£®ZŹĒČĖĢåŃŖŗģµ°°×ÖŠ“ęŌŚµÄ½šŹōŌŖĖŲ£®ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
V”¢W”¢X”¢Y”¢ZŹĒĪåÖÖ³£¼ūŌŖĖŲ£¬ĘäÖŠV”¢W”¢X”¢YĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼1Ź¾£ŗV”¢WµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļM”¢N»ģŗĻŹ±ÓŠ°×ŃĢÉś³É£¬MÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£®ZŹĒČĖĢåŃŖŗģµ°°×ÖŠ“ęŌŚµÄ½šŹōŌŖĖŲ£®ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ £Ø2011?ŗž±±Ä£Äā£©X”¢Y”¢Z”¢M”¢N”¢KŹĒÓɶĢÖÜĘŚŌŖĖŲ¹¹³ÉµÄĪ¢Į££¬ĘäÖŠX”¢Y”¢ZŹĒŃōĄė×Ó£¬M”¢NŹĒÖŠŠŌ·Ö×Ó£¬KŹĒŅõĄė×Ó£¬ĖüĆĒ¾ßÓŠĻĀĮŠ½į¹¹ĢŲµćŗĶŠŌÖŹ£ŗ
£Ø2011?ŗž±±Ä£Äā£©X”¢Y”¢Z”¢M”¢N”¢KŹĒÓɶĢÖÜĘŚŌŖĖŲ¹¹³ÉµÄĪ¢Į££¬ĘäÖŠX”¢Y”¢ZŹĒŃōĄė×Ó£¬M”¢NŹĒÖŠŠŌ·Ö×Ó£¬KŹĒŅõĄė×Ó£¬ĖüĆĒ¾ßÓŠĻĀĮŠ½į¹¹ĢŲµćŗĶŠŌÖŹ£ŗ

