
题目列表(包括答案和解析)
(1)淀粉水解的最终产物是________,用________可以检验淀粉水解是否完全.蛋白质水解的最终产物是________,提纯蛋白质可以采用的一种方法是________(填“盐析”或“过滤”).
(2)①运用化学知识可以解决许多实际问题.下表中完全正确的一组是________(填字母).

②下列有关水资源保护的说法中,不正确的是________(填字母).
a.重金属离子对人体有毒害,可采用沉淀反应除去之
b.化肥中含有植物营养素,可大量使用以改善水环境
c.轧钢厂排出的含盐酸的废水,可用熟石灰中和处理
d.天然水中的细小悬浮颗粒,可用明矾等混凝剂净化
③一般把pH小于5.6的雨水(包括雨、雪、雾、雹等)称为酸雨,酸雨危害极大.下列能减少酸雨产生的有效措施是________(填字母).
A.少用煤作燃料
B.加大石油、煤炭的开采速度,增加化石燃料的供应量
C.燃料脱硫
D.在已酸化的土壤中加入石灰
E.开发新能源
a.ABE b.ACE c.BCD d.CDE
④“垃圾是放错了地方的资源”,应分类回收利用.生活中废弃的塑料袋、废纸、旧橡胶制品等属于________(填字母).
a.盐类 b.糖类 c.无机物 d.有机物
⑤维生素可根据其溶解性的不同分为水溶性维生素和脂溶性维生素两大类.维生素C属于________性维生素,由于它能防治坏血病,又称为抗坏血酸.
⑥黄瓜中含有多种营养成分,尤其是维生素C和B的含量比西瓜高出1~5倍.已知高温时维生素会被破坏,维生素C在酸性环境时较稳定.根据上述内容,你认为应如何合理的食用黄瓜?________.
⑦市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐.此反应的化学反应方程式为________.
| a. | 物质存放 | b. | 区分常见物质 |
| 钢铁防锈--放在干燥空气中 海鲜防腐--用福尔马林浸泡 |
食盐和纯碱--比较颜色 棉线和毛线--点燃并闻气味 | ||
| c. | 物质用途 | d. | 日常生活经验 |
| NaHCO3--用作抗酸类药物 SiO2--用作光导纤维 |
合金--不能作保险丝 醋--可作调味剂和防腐剂 |
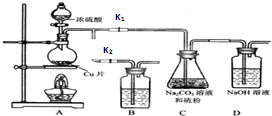 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在;硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得.已知:Na2S2O3在酸性溶液中不能稳定存在;硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I-.
| ||
| ||
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |

 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。 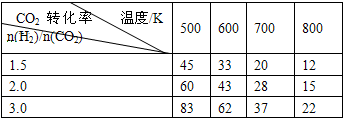


 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。 

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com