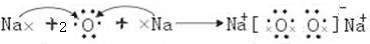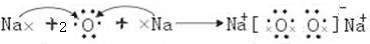(Ⅰ)下表是元素周期表的一部分,针对表中的①~⑥种元素,填写下列空白:
| 族周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 1 |
|
|
|
|
|
|
|
|
| 2 |
|
|
|
① |
|
|
|
|
| 3 |
② |
|
③ |
④ |
|
|
⑤ |
⑥ |
(1)在这些元素中,单质的化学性质最不活泼的是
Ar
Ar
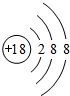
(填具体元素符号).原子结构示意图为
.
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
HClO4
HClO4
,碱性最强的化合物的电子式是
.
(3)最高价氧化物是两性氧化物的元素是
Al
Al
(填具体元素符号);写出它的氧化物与氢氧化钠反应的化学方程式
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.
(4)①和④两元素分别形成的最高价氧化物中,熔点较高的是
SiO2
SiO2
(填具体化学式).
(5)科学家借助元素周期表研究合成有特定性质的新物质,如在
金属与非金属交界处
金属与非金属交界处
寻找半导体材料.
(Ⅱ)化学与我们日常生活中的吃、穿、住、行、医关系密切,其中油脂、淀粉、蛋白质是我们食物中提供能量的主要物质.请按要求回答下列问题(填名称):
(1)油脂在酸性条件下水解的最终产物是
高级脂肪酸
高级脂肪酸
和
甘油
甘油
.
(2)淀粉水解的最终产物是
葡萄糖
葡萄糖
.若要检验淀粉在淀粉酶作用下已经发生了水解,可取少量上述溶液加入
新制氢氧化铜或银氨溶液
新制氢氧化铜或银氨溶液
,加热后再根据实验现象判断;若要检验淀粉没有完全水解,可取少量上述溶液加入几滴
碘水
碘水
,应观察到出现蓝色.
(3)蛋白质在一定条件下能发生水解反应,最终转化为
氨基酸
氨基酸
.


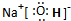
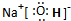
 ?
?