
题目列表(包括答案和解析)
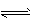 2NH3(g) △H = -92.4 kJ . mol-1。
2NH3(g) △H = -92.4 kJ . mol-1。 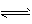 4NO(g)+6H2O(g),反应过程中合金始终保持红热,该反应的化学平衡常数K的表达式为 ____,当升高温度时,K值___(填“增大”、“减小”或“不变”)。NH3的转化率在温度T1下随反应时间(t)的变化如图所示。其他条件不变,仅改变温度为T2(T2大于T1),在框图中用虚线画出温度T2下NH3的转化率随反应时间变化的预期结果示意图。
4NO(g)+6H2O(g),反应过程中合金始终保持红热,该反应的化学平衡常数K的表达式为 ____,当升高温度时,K值___(填“增大”、“减小”或“不变”)。NH3的转化率在温度T1下随反应时间(t)的变化如图所示。其他条件不变,仅改变温度为T2(T2大于T1),在框图中用虚线画出温度T2下NH3的转化率随反应时间变化的预期结果示意图。 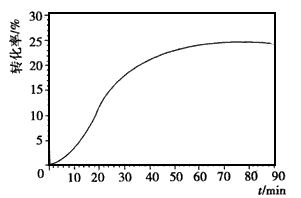

| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
A、反应N2(g)+3H2(g)
| |||||
| B、化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 | |||||
| C、对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 | |||||
| D、将AgNO3溶液和KCl溶液混合后,若c(Ag+)?c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
|
化学反应原理中涉及很多常数,下列说法错误的是 | |
| [ ] | |
A. |
反应N2(g)+3H2(g) |
B. |
化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 |
C. |
对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 |
D. |
将AgNO3溶液和KCl溶液混合后,若c(Ag+)·c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
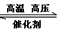 2NH3(g) ΔH<0 具有重要的意义。
2NH3(g) ΔH<0 具有重要的意义。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com