
题目列表(包括答案和解析)
铁的氧化物有多种用途。请解答下面有关问题:
(1)赤铁矿的主要成分是Fe2O3,是工业炼铁的主要原料之一。写出由Fe2O3制得单质铁的化学方程式____________。某赤铁矿除了含Fe2O3之外,还含有少量的SiO2和Al2O3。将试样溶于NaOH溶液,充分反应后过滤,即可得到较纯净的Fe2O3。该过程中发生反应的离子方程式是____________。
(2)Fe2O3可以与铝粉组成铝热剂用于焊接钢轨或定向爆破。某同学猜测,该反应所得熔融物中含有Fe2O3。他设计如下实验来验证自己的猜想:取少量试样,加入足量稀盐酸,然后滴加KSCN溶液,若出现红色,证明含有Fe2O3。否则,不含有Fe2O3。你认为该方案合理吗?
为什么?
铁的氧化物可用于脱除煤气中的H2S,有关反应原理如下:
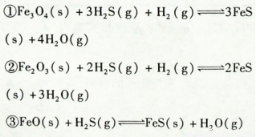
温度与上述各反应的平衡常数的关系如图所示。下列有关说法正确的是
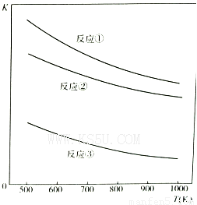
A.反应①、②、③中铁的氧化物都是氧化剂???????????
B.反应①、②、③的正反应都是放热反应
C.反应①、②、③中,温度越高H2S的的脱除率越高???
D.反应①、②、③中,压强越大H2S脱除率越高
铁的氧化物可用于脱除煤气中的H2S,该反应原理为:
①Fe3O4
(s)+3H2S(g)+H2 (g) 3FcS(s)+4H2O(g)
△H=a kJ • mol-1
3FcS(s)+4H2O(g)
△H=a kJ • mol-1
②Fe2O3(s)+2H2S(g)
+ H2(g) 2FeS(s)+3H2O(g)
△H=bkJ • mol-1
2FeS(s)+3H2O(g)
△H=bkJ • mol-1
③FeO(s)+H2S(g)  FeS(s)+H2O(g)
△H=ckJ· mol-1
FeS(s)+H2O(g)
△H=ckJ· mol-1
温度与平衡常数的关系如图,下列有关说法正确的是

A.a、b、c均小于0
B.压强越大,H2S的脱除率越高
C.温度越高,H2S的脱除率越高
D.反应①、②、③的平衡常数表达式相同
铁的氧化物可用于脱除煤气中的H2S,有关反应原理如下: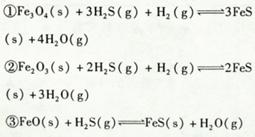
温度与上述各反应的平衡常数的关系如图所示。下列有关说法正确的是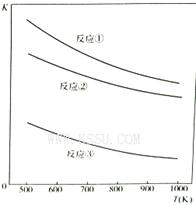
| A.反应①、②、③中铁的氧化物都是氧化剂 |
| B.反应①、②、③的正反应都是放热反应 |
| C.反应①、②、③中,温度越高H2S的的脱除率越高 |
| D.反应①、②、③中,压强越大H2S脱除率越高 |
铁的氧化物可用于脱除煤气中的H2S,该反应原理为:
①Fe3O4 (s)+3H2S(g)+H2 (g) 3FcS(s)+4H2O(g) △H=a kJ ? mol-1
3FcS(s)+4H2O(g) △H=a kJ ? mol-1
②Fe2O3(s)+2H2S(g) + H2(g) 2FeS(s)+3H2O(g) △H=bkJ ? mol-1
2FeS(s)+3H2O(g) △H=bkJ ? mol-1
③FeO(s)+H2S(g)  FeS(s)+H2O(g) △H=ckJ· mol-1
FeS(s)+H2O(g) △H=ckJ· mol-1
温度与平衡常数的关系如图,下列有关说法正确的是
| A.a、b、c均小于0 |
| B.压强越大,H2S的脱除率越高 |
| C.温度越高,H2S的脱除率越高 |
| D.反应①、②、③的平衡常数表达式相同 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com