
题目列表(包括答案和解析)
 《化学反应原理》
《化学反应原理》
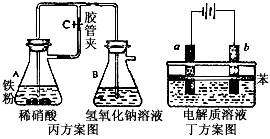
I、已知反应:
3I-(aq)+S2O82-(aq) ![]() I3-(aq)+2SO42-(aq);
I3-(aq)+2SO42-(aq);
(1)写出反应的平衡常数表达式
 K= 。
K= 。
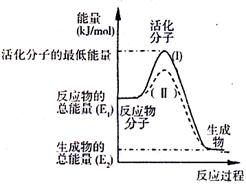
(2)右图表示反应过程中有关物质的能量,则反应
的 △H 0(填>、<、=)。
(I)、(II)两线中,使用催化剂的是 线。
(3)反应中发生反应的I-与被氧化的I-的物质的量比为 。
(4)反应的速率可以用I3-与加入的淀粉溶液反应是蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,记录的数据如下:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-/mol·L-1) | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
则:该实验的目的是
显色时间t1= s
分析表中数据,得出的结论是
II、二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) ![]() 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。
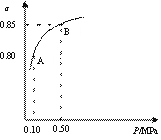 根据图示回答下列问题。
根据图示回答下列问题。
①平衡状态由A变到B时,平衡常数K(A) K(B)
(填“>”、“<”、“=”)。
②已知上述反应的是放热反应,当该反应处于平衡状态时,
在体积不变的条件下,下列选项中有利于提高SO2平衡转
化率的有 (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
E.加入催化剂 F.移出氧气
某兴趣小组设计并进行了以下实验来制取氯水,并利新制用氯水完成实验。
(1)实验室拟用下列装置制备氯水,请按照气体从左向右流动的方向将仪器进行连接:
H→ _____________(填接口处的符号);广口瓶Ⅱ中的试剂为 。

(2)写出该实验中制取Cl2的化学方程式为:___________________________________
(3)某兴趣小组设计实验除去氯化钾中含有Fe3+、SO42-、Br-等杂质离子,步骤如下:
A.溶解,在所得溶液中加入试剂至Fe3+、SO42-沉淀完全,煮沸;
B.过滤,在滤液中加入盐酸调节pH;
C.加入_____(除Br-);蒸干灼烧。请回答问题:
(3)①步骤a中,依次加入的试剂是NH3.H2O、_________、_________。
②步骤c中加入的试剂是__________________。
(4)某研究性学习小组用KSCN检验FeSO4溶液中的Fe2+时,加入过量浓HNO3,溶液的颜色变红。但是将红色溶液放置一会则发现溶液由红色突然变为蓝色,并产生红棕色气体。对这一奇特现象同学们进行了以下探究。
[查阅资料]:
(SCN)2称为拟卤素,性质与卤素单质相似,(SCN)2、Cl2、Br2、I2四种物质的氧化性强弱为:Cl2>Br2>(SCN)2>I2。
[提出假设]:
①甲同学假设是FeSO4与HNO3作用;乙同学假设是______与HNO3作用。
[实验验证]:
②大家经过理性分析,认为甲同学的假设不成立。理由是________________________。
③根据乙同学的假设,设计了如下实验方案进行验证:向浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深色,突然剧烈反应产生大量气泡,放出红棕色气体。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种气体(是空气中的主要成分之一);向反应后的溶液中加入BaCl2溶液产生白色沉淀。
则反应中产生的气体是:_______________________________
[实验结论]:乙同学假设正确。
[实验反思]:
④由实验可知:用SCN-间接检验Fe2+时,加入的氧化剂除用HNO3外还可以选择氯水等,通过该实验探究可知加入氧化剂的量必须要_______(填“少量”、“过量”)。
某兴趣小组设计并进行了以下实验来制取氯水,并利新制用氯水完成实验。
(1)实验室拟用下列装置制备氯水,请按照气体从左向右流动的方向将仪器进行连接:
H→ _____________(填接口处的符号);广口瓶Ⅱ中的试剂为 。
(2)写出该实验中制取Cl2的化学方程式为:___________________________________
(3)某兴趣小组设计实验除去氯化钾中含有Fe3+、SO42-、Br-等杂质离子,步骤如下:
A.溶解,在所得溶液中加入试剂至Fe3+、SO42-沉淀完全,煮沸;
B.过滤,在滤液中加入盐酸调节pH;
C.加入_____(除Br-);蒸干灼烧。请回答问题:
(3)①步骤a中,依次加入的试剂是NH3.H2O、_________、_________。
②步骤c中加入的试剂是__________________。
(4)某研究性学习小组用KSCN检验FeSO4溶液中的Fe2+时,加入过量浓HNO3,溶液的颜色变红。但是将红色溶液放置一会则发现溶液由红色突然变为蓝色,并产生红棕色气体。对这一奇特现象同学们进行了以下探究。
[查阅资料]:
(SCN)2称为拟卤素,性质与卤素单质相似,(SCN)2、Cl2、Br2、I2四种物质的氧化性强弱为:Cl2>Br2>(SCN)2>I2。
[提出假设]:
①甲同学假设是FeSO4与HNO3作用;乙同学假设是______与HNO3作用。
[实验验证]:
②大家经过理性分析,认为甲同学的假设不成立。理由是________________________。
③根据乙同学的假设,设计了如下实验方案进行验证:向浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深色,突然剧烈反应产生大量气泡,放出红棕色气体。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种气体(是空气中的主要成分之一);向反应后的溶液中加入BaCl2溶液产生白色沉淀。
则反应中产生的气体是:_______________________________
[实验结论]:乙同学假设正确。
[实验反思]:
④由实验可知:用SCN-间接检验Fe2+时,加入的氧化剂除用HNO3外还可以选择氯水等,通过该实验探究可知加入氧化剂的量必须要_______(填“少量”、“过量”)。
2008.3
一、选择题(每小题4分,共60分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
C
D
C
C
D
B
D
A
D
C
B
C
D
B
A
二、选择题(每小题4分,选对但不全得2分,共28分)
题号
16
17
18
19
20
21
22
答案
AB
D
B
BCD
B
BD
D
23.(1)3 4;6;2(前3空各1分,最后一空2分)
(2)① (1分)
(1分)
②左(2分)
③电源 电压过低 线圈匝数过少 弹簧劲度系数太大(共3分,答对一条得2分,答对2条得3分)
电压过低 线圈匝数过少 弹簧劲度系数太大(共3分,答对一条得2分,答对2条得3分)
24.(16分)
(1)设小球刚刚进入电场时,竖直方向的速度为 ,则
,则 (2分)
(2分)
设小球在电场中做直线运动时,运动方向与水平方向夹角为 ,
,
则 (2分)
(2分)

 (2分)
(2分)
(2)小球平抛运动过程的时间为 ,则
,则
 (2分)
(2分)
进入电场后,在水平方向上,

 (2分)
(2分)
 (1分)
(1分)
(或设B点到极板上端的距离为L,则 在竖直方向上:
在竖直方向上: )
)
(3)小球到达B点时的水平速度 (2分)
(2分)
竖直分速度 (2分)
(2分)
 (1分)
(1分)
或从A到B由动能定理知:

25.(18分)
(1)回路中平均电动势 (2分)
(2分)
回路中总电阻 (2分)
(2分)
电荷量 (2分)
(2分)
(2)设 时刻导体棒AB的速度为V
时刻导体棒AB的速度为V  (1分)
(1分)
此时导体棒AB产生电动势为 (1分)
(1分)
安培力 (1分)
(1分)
由牛顿第二定律 (1分)
(1分)
 (2分)
(2分)
(3)AB棒末速度 (1分)
(1分)
由动能定理 (2分)
(2分)

 (1分)
(1分)

 (2分)
(2分)
26.(17分)
(1)红色、厚果皮(2分) 绿:红=1:1(2分) 厚:薄=3:1(2分)(只写比例无对应性状不得分)
(2)基因和环境共同作用(2分)
(3)(方法正确、结果与结论相对应即可得分)
方法一:用纯种小果实普通甜椒与大果实太空甜椒杂交(3分)。
若子代全部为大果实,则太空甜椒基因型为DD(2分);
若子代全部为小果实,则太空甜椒基因型为 (2分);
(2分);
若子代呈现两种性状,则太空甜椒基因型为 (2分)。
(2分)。
方法二:
①用纯种大果实太空甜椒自交(2分)。若子代出现性状分离,则太空甜椒基因型为 (2分);若子代全部为大果实,则太空甜椒的基因型为DD或
(2分);若子代全部为大果实,则太空甜椒的基因型为DD或 (2分)
(2分)
②用纯种小果实普通甜椒与大果实太空甜椒杂交(1分)。若子代全部为大果实,则太空甜椒基因型为DD(1分);若子代全部为小果实,则太空甜椒基因型为 (1分)。
(1分)。
27.(16分)
(1)叶面积指数在 范围内,随叶面积指数的增加,有机物积累增加(1分);叶面积指数超过
范围内,随叶面积指数的增加,有机物积累增加(1分);叶面积指数超过 ,有机物积累量反而下降(1分)。种植农作物要合理密植(2分)
,有机物积累量反而下降(1分)。种植农作物要合理密植(2分)
(2)增加光照,提高温度,提高光合作用效率(1分);夜间降温,能抑制细胞呼吸,减少有机物的消耗,从而有利于有机物的积累,提高产量(1分)。利用农作物秸秆等进行沼气池发酵,利用发酵产生的余热使温室升温(符合题意即可得2分)
(3)①取两只烧杯,编号为A、B,放人等量淀粉糊,在A烧杯中加入 土壤浸入液,B烧杯中加人
土壤浸入液,B烧杯中加人 蒸馏水(2分)。
蒸馏水(2分)。
②在室温下放置一段时间后,分别取A、B烧杯中的溶液 ,各放人两支试管中,分别编号为
,各放人两支试管中,分别编号为 。(2分)
。(2分)
③在 、
、 中各加入碘液,在
中各加入碘液,在 、
、 中各加入斐林试剂。(2分)
中各加入斐林试剂。(2分)
④采取相应措施观察试管中溶液的颜色变化,记录实验结果。(2分)
28.(13分)
(1)坩埚、坩埚钳、泥三角(3分,填对一个给1分,有错误本空为0分);过滤(2分)
(2)步骤Ⅱ中得到溶液的红色比步骤I中得到溶液的红色深(2分)
(3)+2价(2分)
(4) (2分);沉淀部分溶解(2分)
(2分);沉淀部分溶解(2分)
29.(13分)
(1) (3分)
(3分)
(2)① (2分)
(2分)
②[Na+]>[S2-]>[OH-]>[H+](3分)
(3) ① (2分)
(2分)
②N>0>H或N、O、H(3分)
30.(16分)
(1) (2分,不写单位扣1分)
(2分,不写单位扣1分)
(2)减小压强(2分); (2分,不写单位扣1分);
(2分,不写单位扣1分);
0.84(2分); (2分)
(2分)
(3)

(3分,不写可逆号、热量表示错误各扣1分)
(4) (3分,写对2个3分,对1个给1分)
(3分,写对2个3分,对1个给1分)
【选做部分】
31.(8分)【化学―化学与技术】
(1)稀释 以防爆炸。(1分)
以防爆炸。(1分)
(2) (2分);
(2分);
 (1分)
(1分)
(3)连续测定吸收塔内溶液的 (1分)
(1分)
(4)蒸发、结晶、过滤(3分,答对一个给1分)
32.(8分)【化学一物质结构与性质】
(1) ;
; (各1分,共2分)
(各1分,共2分)
(2)直线型; 低;  为分子晶体,
为分子晶体, 为原子晶体(各1分,共3分)
为原子晶体(各1分,共3分)
(3) ; 2(各1分,共2分)
; 2(各1分,共2分)
(4)B(1分)
33.(8分)【化学―有机化学基础】
(1)  ;
; (各1分,共2分)
(各1分,共2分)
(2)加成反应; 缩聚反应(各1分,共2分)
(3)②
(2分,条件错误扣1分)
④
(2分,条件错误扣1分)
34.(8分)【生物一生物技术实践】
(1)提供碳源、氮源、磷酸盐和维生素
(2)添加高浓度糖 将培养基的 调至酸性 琼脂(凝固剂)
调至酸性 琼脂(凝固剂)
(3)灭菌 保证每次划线时接种环上的酵母菌来自上一划线的末端(1分);通过增加划线次数使酵母菌数目逐渐减少,最后得到由单个细胞繁殖而来的菌落(1分)。
(4)挑选葡萄 冲洗
冲洗 榨汁
榨汁 酒精发酵
酒精发酵 果酒
果酒
35.(8分)【生物―现代生物科技专题】
(1)纤维素酶和果胶酶 无菌 愈伤
(2)免疫处理的B淋巴细胞和骨髓瘤细胞 抗生素、血清、血浆等 既能迅速繁殖,又能产生专一的抗体
(3)克服远缘杂交不亲和的障碍 灭活的病毒
36.(8分)
(1)在冰水混合物中时,被封气体发生等温变化
 (1分)
(1分)

 (1分)
(1分)
又 (1分)
(1分)
 (1分)
(1分)
(2)当被封气体温度变为 时,气体发生等压变化
时,气体发生等压变化

其中

 (2分)
(2分)
37.(8分)
(1)在波的传播方向上,各质点起振方向都相同,与此时刻 处质点振动方向相同,沿
处质点振动方向相同,沿 轴负方向.
(2分)
轴负方向.
(2分)
(2)由波的图像可得波长 ,P点第一次到达波谷时间即为P点前方距P点最近的波谷传播到P所用时间
,P点第一次到达波谷时间即为P点前方距P点最近的波谷传播到P所用时间 (3分)
(3分)
(3)
 P、Q两质点振动情况相反
P、Q两质点振动情况相反
 当P到波峰时,Q质点在波谷. (3分)
当P到波峰时,Q质点在波谷. (3分)
38.(8分)
(1): (3分)
(3分)
(2)衰变时满足动量守恒: (1分)
(1分)
已知:
 (1分)
(1分)
 (1分)
(1分)
又 (1分)
(1分)
 (1分)
(1分)
天星教育网(www.tesoon.com) 版权所有
天星教育网(www.tesoon.com) 版权所有
天星教育网(www.tesoon.com) 版权所有
| ||||||||||||||||||||||||||||||||||