
题目列表(包括答案和解析)


 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| O | 2- 3 |
| 净含量:500mL | |
| 饮用水矿物质成分(mg.L-1) | |
| 钙Ca | ≥4.0 |
| 镁Mg | ≥1.0 |
| 钠Na | ≥3.0 |
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为
A.0.1 mol/L B.0.2 mol/L C.0.3 mol/L D.0.4 mol/L
现有200mL MgCl2、AlCl3的混合液,其中c(Mg2+)=0.2mol·L-1,c(Cl-)="1.3" mol·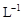 。要使Mg2+转化成Mg(OH)2,并使Mg2+和Al3+分离开来,至少需要4
mol·L-1的NaOH溶液
。要使Mg2+转化成Mg(OH)2,并使Mg2+和Al3+分离开来,至少需要4
mol·L-1的NaOH溶液
A.140mL B.120mL C.100mL D.80mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com