
题目列表(包括答案和解析)
下列关于热化学反应的描述中正确的是 ( )
A.HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H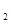 SO
SO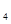 和Ca(OH)
和Ca(OH)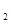 反应的中和热△H=2×(-57.3)kJ/mol
反应的中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0 kJ/tool,则2C0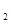 (g)=2CO(g)+0
(g)=2CO(g)+0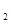 (g)反应的△H=+2x 283.0 Ki/mol
(g)反应的△H=+2x 283.0 Ki/mol
C.反应A(s)+B(g)=C(s)+D(s)能自发进行,则一定有△H>0
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
某恒温密闭容器中,可逆反应A(s)??B+C(g)? ΔH=Q kJ/mol (Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是( )
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q
一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)
A(s)+B(g)  C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
|
容器编号 |
n(B)/mol |
n(C)/mol |
n(D)/mol |
反应时间/min |
反应速率 |
|
Ⅰ |
0.06 |
0.60 |
0.10 |
t1 |
v(正)=v(逆) |
|
Ⅱ |
0.12 |
1.20 |
0.20 |
t2 |
|
|
Ⅲ |
0.32 |
1.0 |
0 |
0 |
|
|
Ⅳ |
0.12 |
0.30 |
|
|
v(正)=v(逆) |
下列说法正确的是 ( )
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ中反应至平衡时吸热20 kJ
D.容器Ⅳ中c(D)= 0.4 mol·L-1
下列说法错误的是
A. 反应A(s)+B(g) === C(s)+D(s)能自发进行,则一定有ΔH <0
B.FeS不溶于水,但能溶于稀盐酸中
C.在滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性
D.常温条件下,相同大小的钠粒在20mL硫酸铜溶液中比在20 mL纯水中反应更剧烈,是因为硫酸铜溶液中的c(H+)比纯水中的大
以下可逆反应中,达到平衡后,通过升高温度可提高反应物转化率的是 ;通过增大压强可提高反应物转化率的是 ;改变压强,转化率不变的是 。
①A(s)+B(g) 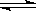 C(g), ΔH
< 0;
C(g), ΔH
< 0;
②N2(g)+3H2(g) 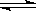 2NH3(g), ΔH < 0;
2NH3(g), ΔH < 0;
③2NO2(g) 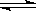 2NO(g) +O2(g),ΔH > 0;
2NO(g) +O2(g),ΔH > 0;
④2SO2(g)+O2(g) 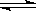 2SO3(g) ,ΔH
< 0。
2SO3(g) ,ΔH
< 0。
⑤CO(g)+NO2(g) 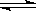 CO2(g) +NO(g),ΔH < 0;
CO2(g) +NO(g),ΔH < 0;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com