
题目列表(包括答案和解析)

a.冰醋酸14.3mL(约0.25mol),b.95%乙醇23mL(约0.37mol),c.浓H2SO4,d.饱和 Na2CO3溶液,e.饱和CaCl2溶液(CaCl2易跟乙醇生成CaCl2·6C2H5OH)。
实验过程主要是将各装置连接好并检查气密性后,进行以下各步骤:
①在蒸馏烧瓶里注入少量乙醇和所需全部浓 H2SO4并混合均匀。在分液漏斗里加入剩下的乙醇和全部冰醋酸并混合均匀。
②用油浴加热,温度保持在130℃~140℃。
③将分液漏斗内液体缓缓滴入蒸馏烧瓶。调节滴入液体速率,使之与馏出酯的滴液速率大致相同,直到加料完毕。
④温度保持一段时间,至没有液体馏出时,停止加热。
⑤取下锥形瓶B,将饱和Na2CO3溶液分批分次加到馏出液里,边加边摇荡至没有气泡产生时为止。
⑥将B中液体在另一分液漏斗中分液,弃去水层。
⑦在分液漏斗油层中加入饱和CaCl2溶液,摇荡后静置,分层分液,弃去水层。油层为粗制乙酸乙酯。
试回答:
(1)配料中的乙醇和乙酸未按物质的量比1∶1配制的理由是________。
(2)浓H2SO4的作用是________。
(3)操作③使加料与馏出液速率大致相等的理由是________。
(4)用饱和Na2CO3溶液洗涤酯的目的是________,用饱和CaCl2溶液洗涤酯的目的是________。
(5)如果同时用Na2CO3与CaCl2两种饱和溶液冼涤酯时,会出现的情况是________。
(6)在粗酯中还杂有的主要有机物是________,产生它的原因是________。
(7)实验时B瓶支管有长导管通向室外的理由是________。
实验室制取乙酸乙酯的装置如图。实验使用的药品如下(烧杯夹持装置、温度计已略去):

a.冰醋酸14.3mL(约0.25mol),b.95%乙醇23mL(约0.37mol),c.浓H2SO4,d.饱和 Na2CO3溶液,e.饱和CaCl2溶液(CaCl2易跟乙醇生成CaCl2·6C2H5OH)。
实验过程主要是将各装置连接好并检查气密性后,进行以下各步骤:
①在蒸馏烧瓶里注入少量乙醇和所需全部浓 H2SO4并混合均匀。在分液漏斗里加入剩下的乙醇和全部冰醋酸并混合均匀。
②用油浴加热,温度保持在130℃~140℃。
③将分液漏斗内液体缓缓滴入蒸馏烧瓶。调节滴入液体速率,使之与馏出酯的滴液速率大致相同,直到加料完毕。
④温度保持一段时间,至没有液体馏出时,停止加热。
⑤取下锥形瓶B,将饱和Na2CO3溶液分批分次加到馏出液里,边加边摇荡至没有气泡产生时为止。
⑥将B中液体在另一分液漏斗中分液,弃去水层。
⑦在分液漏斗油层中加入饱和CaCl2溶液,摇荡后静置,分层分液,弃去水层。油层为粗制乙酸乙酯。
试回答:
(1)配料中的乙醇和乙酸未按物质的量比1∶1配制的理由是________。
(2)浓H2SO4的作用是________。
(3)操作③使加料与馏出液速率大致相等的理由是________。
(4)用饱和Na2CO3溶液洗涤酯的目的是________,用饱和CaCl2溶液洗涤酯的目的是________。
(5)如果同时用Na2CO3与CaCl2两种饱和溶液冼涤酯时,会出现的情况是________。
(6)在粗酯中还杂有的主要有机物是________,产生它的原因是________。
(7)实验时B瓶支管有长导管通向室外的理由是________。
某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。
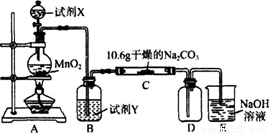
(1)写出装置A中发生反应的离子方程式:
(2)写出试剂Y的名称:_____________________。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。可以确定的是C中含有的氯盐只有一种,且含有NaHCO3,现对C成分进行猜想和探究。
①提出合理假设:
假设一:存在两种成分: NaHCO3和__________
假设二:存在三种成分: NaHCO3和__________、___________。
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
|
实验步骤 |
预期现象和结论 |
|
步骤1:取C中的少量固体样品于试管中,滴加 足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。 |
|
|
步骤2:向A试管中滴加______________: |
①若无明显现象,证明固体中不含碳酸钠; ②若溶液变浑浊,证明固体中含有碳酸钠。 |
|
步骤3:向B试管中滴加______________: |
若溶液变浑浊,结合步骤2中的①,则假设 一成立:结合步骤2中的②,则假设二成立。 |
(4)己知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为 。
(5)常温下Na2CO3和NaHCO3均为0.1mol/L的混合溶液中,c(OH﹣)-c(H+)=___________(用含碳元素的粒子浓度表示),在该溶液中滴加稀盐酸至中性时,溶液中溶质的成分有______________________。
某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。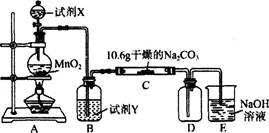
(1)写出装置A中发生反应的离子方程式:
(2)写出试剂Y的名称:_____________________。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。可以确定的是C中含有的氯盐只有一种,且含有NaHCO3,现对C成分进行猜想和探究。
①提出合理假设:
假设一:存在两种成分: NaHCO3和__________
假设二:存在三种成分: NaHCO3和__________、___________。
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加 足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。 | |
| 步骤2:向A试管中滴加______________: | ①若无明显现象,证明固体中不含碳酸钠; ②若溶液变浑浊,证明固体中含有碳酸钠。 |
| 步骤3:向B试管中滴加______________: | 若溶液变浑浊,结合步骤2中的①,则假设 一成立:结合步骤2中的②,则假设二成立。 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com