(2011?双流县模拟)I.硫酸铁糖衣药片是一种治疗缺铁性贫血的药剂.某化学课外活动小组测定其中铁元素含量的实验步骤如下:

(1)刮除药片糖衣称得样品ag,将其研碎后迅速溶解,配制溶液.操作如图所示,操作是否正确,
不正确
不正确
,如不正确,说明原因(正确可不填写)

(2)洗涤的目的是除去附着在沉淀上的
NH4+、Cl-、SO42-、OH-、
NH4+、Cl-、SO42-、OH-、
.(写离子符号)
(3)将沉淀物灼烧,冷却至室温,称得其质量为b
1g,再次灼烧并冷却至室温称得其质量为b
2 g,若b
1-b
2=0.3,则接下来的操作
再次加热,并置于干燥器中冷却,称量,直至两次质量差不超过0.1克为止
再次加热,并置于干燥器中冷却,称量,直至两次质量差不超过0.1克为止
,后通过计算可得出结果.
(4)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
(用化学方程式表示)
II.某化学兴趣小组在做实验时,将AgNO
3溶液和KI溶液混合,发现有黄色沉淀生成,振荡后迅速消失.大家经查阅资料后发现,可能的原因是发生了下列反应:AgI+I
-
[AgI
2]
-(1)甲同学设计了两个简单的实验方案来进行验证,请你协助他完成实验.
实验l:向浓Ⅺ溶液中滴加AgNO
3溶液,观察到无沉淀生成.
实验2:向AgNO
3溶液中滴加Ⅺ溶液,有黄色沉淀生成;再
继续滴加KI溶液,黄色沉淀溶解
继续滴加KI溶液,黄色沉淀溶解
.
(2)乙同学在实验所得的溶液中滴加硝酸溶液,结果又出现了沉淀.请解释出现沉淀的原因
加入硝酸溶液后,硝酸将碘离子氧化,使碘离子浓度减小,平衡AgI+I-?[AgI2]-逆向移动
加入硝酸溶液后,硝酸将碘离子氧化,使碘离子浓度减小,平衡AgI+I-?[AgI2]-逆向移动
.
(3)丙同学在实验所得的溶液中,滴加氯水也可以看到沉淀,但由于溶液为黄色,分不清沉淀的颜色.大家通过查阅数据,分析认为产生的沉淀不可能是AgCl,所查阅的数据是
AgI、AgCl的溶解度
AgI、AgCl的溶解度
.
同学们通过查阅资料知道,AgCl沉淀能溶于浓氨水.请写出这一反应的离子方程式
AgCl+2NH3?H2O=[Ag(NH3)2]++Cl-+2H2O;
AgCl+2NH3?H2O=[Ag(NH3)2]++Cl-+2H2O;
.



 [AgI2]-
[AgI2]-
 (2011?安徽)科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
(2011?安徽)科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )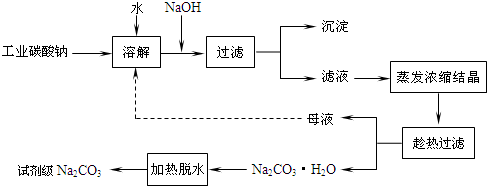
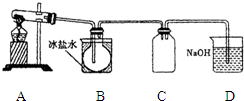 室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;