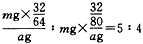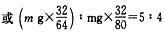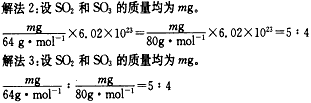ЃЈ2009?ИЇЫГФЃФтЃЉЙЄвЕЩЯЩњВњСђЫсЪБЃЌРћгУДпЛЏбѕЛЏЗДгІНЋSO
2зЊЛЏЮЊSO
3ЪЧвЛИіЙиМќВНжшЃЎбЙЧПМАЮТЖШЖдSO
2зЊЛЏТЪЕФгАЯьШчЯТБэЃЈдСЯЦјИїГЩЗжЕФЬхЛ§ЗжЪ§ЮЊЃКSO
2ЃК7% O
2ЃК11% N
2ЃК82%ЃЉЃЛ
бЙЧП/MPa
зЊЛЏТЪ/%
ЮТЖШ/Ёц |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2 |
99.6 |
99.7 |
99.9 |
| 500 |
93.5 |
96.9 |
97.8 |
99.3 |
| 600 |
73.7 |
85.8 |
89.5 |
96.4 |
ЃЈ1ЃЉвбжЊSO
2ЕФбѕЛЏЪЧЗХШШЗДгІЃЌШчКЮРћгУБэжаЪ§ОнЭЦЖЯДЫНсТлЃП
бЙЧПвЛЖЈЪБЃЌЮТЖШЩ§ИпЪБЃЌSO2ЕФзЊЛЏТЪНЕЕЭЃЌЫЕУїЩ§ИпЮТЖШгаРћгкЦНКтЯђФцЗДгІвЦЖЏЃЌЙЪе§ЗДгІЮЊЗХШШЗДгІ
бЙЧПвЛЖЈЪБЃЌЮТЖШЩ§ИпЪБЃЌSO2ЕФзЊЛЏТЪНЕЕЭЃЌЫЕУїЩ§ИпЮТЖШгаРћгкЦНКтЯђФцЗДгІвЦЖЏЃЌЙЪе§ЗДгІЮЊЗХШШЗДгІ
ЃЛ
ЃЈ2ЃЉдкДѓ400ЁЋ500ЁцЪБЃЌSO
2ЕФДпЛЏбѕЛЏВЩгУГЃбЙЖјВЛЪЧИпбЙЃЌжївЊдвђЪЧЃК
діДѓбЙЧПЖдSO2ЕФзЊЛЏТЪгАЯьВЛДѓЃЌЭЌЪБдіДѓГЩБО
діДѓбЙЧПЖдSO2ЕФзЊЛЏТЪгАЯьВЛДѓЃЌЭЌЪБдіДѓГЩБО
ЃЛ
ЃЈ3ЃЉбЁдёЪЪвЫЕФДпЛЏМСЃЌЪЧЗёПЩвдЬсИпSO
2ЕФзЊЛЏТЪЃП
Зё
Зё
ЃЈЬюЁАЪЧЁБЛђЁАЗёЁБЃЉЃЌЪЧЗёПЩвддіДѓИУЗДгІЫљЗХГіЕФШШСПЃП
Зё
Зё
ЃЈЬюЁАЪЧЁБЛђЁАЗёЁБЃЉЃЛ
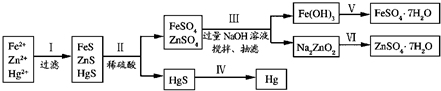
ЃЈ4ЃЉЙЄвЕЩњВњСђЫсВњЩњЕФЮВЦјжївЊКЌSO
2КЭSO
3ЃЌЛсдьГЩ
Ысгъ
Ысгъ
ЃЈЬюЛЗОГЮЪЬтЃЉЃЌЙЄвЕЩЯГЃгУзуСПЕФХЈАБЫЎРДЮќЪеЃЌаДГіЯрЙиЕФРызгЗНГЬЪН
2NH3?H2O+SO2=2NH4++SO32-+H2O
2NH3?H2O+SO2=2NH4++SO32-+H2O
2NH3?H2O+SO3=2NH4++SO42-+H2O
2NH3?H2O+SO3=2NH4++SO42-+H2O
ЃЈ5ЃЉвбжЊЃК2SO
2ЃЈgЃЉ+O
2ЃЈgЃЉ=2SO
3ЃЈgЃЉЃЛЁїH=-196.9kJ?mol
-1ЃЌМЦЫуУПЩњВњ1ЭђЖж98%СђЫсЫљашвЊЕФSO
3жЪСПКЭгЩSO
2ЩњВњетаЉSO
3ЫљЗХГіЕФШШСПЃЎЃЈаДГіНтЬтЙ§ГЬЃЉ