
题目列表(包括答案和解析)
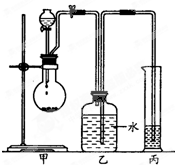 某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.
某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.| 实验编号 | 有机样品的体积 | 有机样品的质量 | 生成气体的体积(标准状况下) | I | 3.65mL | 3.8g | 1120mL | II | 7.30mL | 7.6g | 2240mL | III | 14.60mL | 15.2g | 4000mL |
下图是一些物质间的转化关系图,图中所有物质含有的元素中只有一种不是短周期元素,所有反应物、生成物及溶液中的水以及部分反应中一些生成物未标出。C、D、E、K为单质,N为两性化合物。J是由两种元素组成的和SiC相同晶体类型的新型材料,且J和SiC具有相同的价电子数和原子数。I是由四种元素组成的强碱。反应③用于检验一种常见的有机官能团,反应⑤、⑥用于工业中生产B。

回答下列问题:
(1)写出下列物质的化学式:G 、I 。
(2)写出反应①、⑦的离子方程式:
① ,
⑦ ;
(3)J和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料。反应②是日本科学家研究开发制备该纳米级复合粉末的最新途径。已知反应②中n(F)∶n(E)∶n(J)∶n(SiC)∶n(K)=1∶2∶4∶1∶3,写出反应②的化学方程式 。
(08衡阳八中模拟)(10分)烷烃A只可能有三种一氯取代产物B、C和D。C的分子式是C6H13Cl,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。有关物质间的转化关系如下图所示。

(1)A的结构简式是 。
(2)F具有的官能团名称是 。
(3)B转变为F的反应属 反应,B转变为E的反应属于 反应。
(4)D→E的化学反应方程式 。
(5)①反应的化学反应方程式 。
(6)1.16 g H与足量NaHCO3作用,标准状况下可得CO2的体积是 mL。
 ;
;
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com