
题目列表(包括答案和解析)
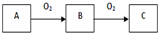 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去).
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去).
| ||
| ||
| ||
| ||

| 催化剂 |
| 加热 |
| 催化剂 |
| 加热 |



| ||
| △ |
| ||
| △ |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
| ||
| ||
(18分)A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
⑴ 若A是一种黄色单质固体,则B→C的化学方程式为 。
⑵ 若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,C可用在矿山、坑道、潜水或宇宙飞船等缺氧的场合,将人们呼出的CO2再转换成O2,以供呼吸之用,请用化学方程式表示该反应原理 。
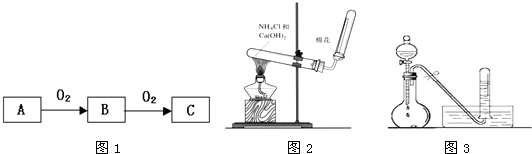
⑶若A为能使湿润的红色石蕊试纸变蓝的气体,C是红棕色气体,且B和C易在空气形成光化学烟雾。
①则A为 ,C为 ,(填写化学式)
实验室用熟石灰与氯化铵固体共热制取A,写出此化学方程式: 。
②写出C与水反应的化学方程式: 。
一、选择题
1. B 2. C 3. D 4. B 5. B 6. C 7. A 8. A 9. C 10. B 11. D 12. C 13.B
 14.C 15.
BC 16. AB 17. AD 18. ABC 19. B 20. B 21. A
14.C 15.
BC 16. AB 17. AD 18. ABC 19. B 20. B 21. A
实验题:
22.(17分) (1) ①0.10 ;②
b. U2R'/(U1―U2); U1为 v示数, U2为 mV示数,
R′为此时电阻箱的取值。(10分)
23.(15分)(1)物块从A到C过程,由动能定理得
(4分)
将 (4分)
(4分)
(2)∵物块在A、C处速率均为0,且物块在AB、BC上均做匀变速直线运动,
根据 上滑行的平均速度大小相等。(3分)
上滑行的平均速度大小相等。(3分)
 (4分)
(4分)
注:本题用牛顿运动定律、动量定理求解同样参照给分。
24.(18分)(1)最初ab、cd均刚好保持静止。根据其受力情况可知ab、cd与导轨间最大静摩擦力 当用外力F作用ab棒时
当用外力F作用ab棒时 (2分)
(2分)
故ab棒开始沿导轨加速上滑,棒中产生感应电动势,回路中形成感应电流。因此,棒ab又将受到安培力作用。当ab棒所受外力的合力为零时,金属棒ab达最大速度,设为Vm,则
 (2分) 其中
(2分) 其中
 I (2分)
I (2分)
故 考虑此时棒cd的受力情况,应有
考虑此时棒cd的受力情况,应有 仍然保持静止。(2分)
仍然保持静止。(2分)
所以有 (2分) 联立以上方程可得
(2分) 联立以上方程可得 (2分)
(2分)
(2)由以上方程中解得 (3分)
(3分)
则回路所产生的焦耳热
 (3分)
(3分)
25(22分)
解:(1)当有电场和磁场时,应作匀速运动;
F电= F洛=qB1V0 ∴ B1=1.3×10-3T……① 4分
F洛=qB1V0 ∴ B1=1.3×10-3T……① 4分
当只有磁场时,作匀速圆周运动:
R= =6.4×10
=6.4×10 ……②
3分
……②
3分
T= =1.0×10-4S
……③
1分
=1.0×10-4S
……③
1分
t= +3T=3.5×10-4+3.0×10-4=6.5×10-4S
……④ 3分
+3T=3.5×10-4+3.0×10-4=6.5×10-4S
……④ 3分
由U-t图知,粒子能水平穿越两板
故:B1=1.3×10-3T,T=6.5×10-4S 1分
(2)设碰n次,则半周分为n+1个等分圆弧,有:
Q= ……⑤ 2分
……⑤ 2分
tan …… ⑥ 2分
…… ⑥ 2分
Rn= ……⑦
2分
……⑦
2分
联立得:B2= ……⑧ 2分
……⑧ 2分
代入数据: B2=7.5×10-6cot (n=1,2,…) 2分
(n=1,2,…) 2分
26.(15分)
|