
题目列表(包括答案和解析)
温度为500℃时,反应4NH3+5O2  4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率
4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率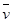 (x)为
(x)为
A、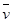 (O2)=0.025 mol·L-1·s-1
B、
(O2)=0.025 mol·L-1·s-1
B、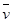 (NO)=0.06 mol·L-1·s-1
(NO)=0.06 mol·L-1·s-1
C、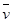 (NH3)=0.002 mol·L-1·s-1 D、
(NH3)=0.002 mol·L-1·s-1 D、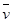 (H2O)=0.03 mol·L-1·s-
(H2O)=0.03 mol·L-1·s-
向4.0 L容器中充入0.70 mol SO2和0.40 mol O2 , 4 s末测得剩余SO2 0.30 mol,则v(O2)为( )
A.0.10 mol·L-1·s-1 B.0.025 mol·L-1·s-1
C.0.50 mol·L-1·s-1 D.0.0125 mol·L-1·s-1
向4.0 L容器中充入0.70 mol SO2和0.40 mol O2,4 s末测得剩余SO2 0.30 mol,则v(O2)为( )
A.0.10 mol·L-1·s-1 B.0.025 mol·L-1·s-1
C.0.50 mol·L-1·s-1 D.0.012 5 mol·L-1·s-1
将混合物A放入密闭容器中加热,在一定条件下存在如下两种平衡:A(s) 2B(g)+C(g)2C(g)
2B(g)+C(g)2C(g) D(g)+3E(g)经测定,这时C的浓度为0.01mol·L-1,E的浓度为0.015 mol·L-1 ,则B的浓度( )
D(g)+3E(g)经测定,这时C的浓度为0.01mol·L-1,E的浓度为0.015 mol·L-1 ,则B的浓度( )
A.0.02 mol·L-1 B.0.025 mol·L-1 C.0.03 mol·L-1 D.0.04mol·L-1
向4.0 L容器中充入0.70 mol SO2和0.40 mol O2 , 4 s末测得剩余SO2 0.30 mol,则v(O2)为( )
| A.0.10 mol·L-1·s-1 | B.0.025 mol·L-1·s-1 |
| C.0.50 mol·L-1·s-1 | D.0.0125 mol·L-1·s-1 |
一、1.B 2.A?
3.解析:v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6。
答案:D?
4.BC 5.B 6.B 7.D 8.BD?
9.解析:由①②组数据解得m=1,由②③组数据解得n= 。
。
答案:D
二、10.(1)0.013 (2)1.0 催化剂 (3)> >
(4)吸热 温度升高时,平衡向右移动?
11.①
12.④>③=②>①?
13.
 (
( -x)?mol?L-1?min-1
-x)?mol?L-1?min-1
14.(1)1∶50 根据勒夏特列原理,通入过量而廉价的氧气,可提高SO2的转化率
(2)废气中每小时排出的SO2的体积为:1
(3)SO2 ~ 2NH3 ~ (NH4)2SO4?
 mol?
mol?
 mol
mol
 mol
mol
故可得(NH4)2SO4: mol×1
mol×1
消耗氨气: mol×2×1
mol×2×1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com