
题目列表(包括答案和解析)
![]()
(1)若A、B起始物质的量均为零,通入C的物质的量(mol)随反应时间(min)的变化情况如下表:
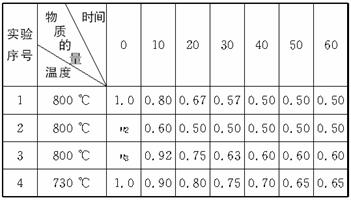
根据上表数据,完成下列填空:
①在实验1中反应在10—20 min内反应的平均速率为 ① mol·(L·min)-1;实验2中采取的措施是 ② ;实验3中n3 ③ 1.0 mol(填“>”“=”或“<”)。
②比较实验4和实验1,可推测该反应中Q ④ 0(填“>”“=”或“<”),理由是 ⑤ 。
(2)在另一反应过程中A(g)、B(g)、C(g)物质的量变化如下图所示,根据图中所示判断下列说法正确的是 ⑥ 。
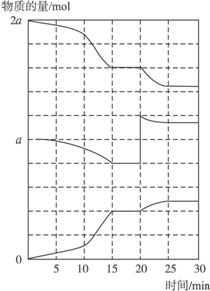
a.10—15 min可能是升高了温度 b.10—15 min可能是加入了催化剂
c.20 min时可能是缩小了容器体积 d.20 min时可能是增加了B的量
(3)一定条件下,向上述容器中通入5 mol A(g)和3 mol B(g),此时容器的压强为p(始)。反应进行并达到平衡后,测得容器内气体压强为p(始)的![]() 。若相同条件下,向上述容器中分别通入a mol A(g)、b mol B(g)、c mol C(g),欲使达到新平衡时容器内气体压强仍为p(始)的
。若相同条件下,向上述容器中分别通入a mol A(g)、b mol B(g)、c mol C(g),欲使达到新平衡时容器内气体压强仍为p(始)的![]() 。
。
①a、b、c必须满足的关系是 ⑦ , ⑧ 。(一个用a、c表示,另一个用b、c表示)
②欲使起始时反应表现为向正反应方向进行,则a的取值范围是 ⑨ 。
| |||||||||||||||
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) |
滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 20.02 | 20.00 |
| 2 | 0.10 | 20.00 | 20.00 |
| 3 | 0.10 | 19.00 | 20.00 |
| 4 | 0.10 | 19.98 | 20.00 |
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) |
滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.1000 | 22.62 | 20.00 |
| 2 | 0.1000 | 22.72 | 20.00 |
| 3 | 0.1000 | 22.80 | 20.00 |
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:| 实验编号 | NaOH溶液的浓度 (mol/L) |
滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
一、1.B 2.A?
3.解析:v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6。
答案:D?
4.BC 5.B 6.B 7.D 8.BD?
9.解析:由①②组数据解得m=1,由②③组数据解得n= 。
。
答案:D
二、10.(1)0.013 (2)1.0 催化剂 (3)> >
(4)吸热 温度升高时,平衡向右移动?
11.①
12.④>③=②>①?
13.
 (
( -x)?mol?L-1?min-1
-x)?mol?L-1?min-1
14.(1)1∶50 根据勒夏特列原理,通入过量而廉价的氧气,可提高SO2的转化率
(2)废气中每小时排出的SO2的体积为:1
(3)SO2 ~ 2NH3 ~ (NH4)2SO4?
 mol?
mol?
 mol
mol
 mol
mol
故可得(NH4)2SO4: mol×1
mol×1
消耗氨气: mol×2×1
mol×2×1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com