
题目列表(包括答案和解析)
(1)写出以上叙述中涉及的化学方程式:
①________________________________________________。
②________________________________________________。
③________________________________________________。
④________________________________________________。
(2)制取甲硅烷的装置与制取________(填“O2”或“H2”)的装置相似。
(3)加入稀盐酸之前应向密闭装置中通入氮气一会儿,其目的是:________________。
(4)收集甲硅烷气体只能采用排水法,这是因为_________________。收集完甲硅烷气体后不能直接将导管从水槽中取出,这是为了防止________。要使制取甲硅烷的实验停止,正确的操作方法是:________________。
碳和硅的性质相似。碳的最简单的氢化物是甲烷,硅的最简单的氢化物称为甲硅烷(SiH4)。甲硅烷是一种无色无味的气体(其密度比空气大),不易溶于水,其化学性质比甲烷活泼。在实验室里制取甲硅烷的方法是:将白净细砂(SiO2)与镁粉混合起来,灼烧到反应物转变为灰黑色的硅化镁(Mg2Si)和白色的氧化镁后冷却到室温;取一定量的灼烧后的残留物,置于制取甲硅烷的装置中,滴加稀盐酸后立即有甲硅烷气体逸出,并迅速地自燃。
(1)写出以上叙述中涉及的化学方程式:
①________________________________________________。
②________________________________________________。
③________________________________________________。
④________________________________________________。
(2)制取甲硅烷的装置与制取________(填“O2”或“H2”)的装置相似。
(3)加入稀盐酸之前应向密闭装置中通入氮气一会儿,其目的是:________________。
(4)收集甲硅烷气体只能采用排水法,这是因为_________________。收集完甲硅烷气体后不能直接将导管从水槽中取出,这是为了防止________。要使制取甲硅烷的实验停止,正确的操作方法是:________________。
(18分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气
写出A、B中所盛放最佳化学试剂的名称 、 ,画出虚线框内所需装置图并标明所需试剂的名称。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②: ;假设③: 。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 |
| 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |
由此得出结论:假设 成立(填序号①②③)。
Ⅲ、为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2]
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
IV、a溶液常作印刷电路铜板的腐蚀剂,写出发生反应的离子方程式 。活动小组的同学们又设计了两种从上述废液中回收Cu的方案:
方案1:设计流程图如下:
请分别写出操作①和试剂②的名称_________,_______。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,铜作________极。当观察到阴极有少量气泡产生时,停止电解,这时要回收的Cu已全部析出。
评价:方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为: 。
(18分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气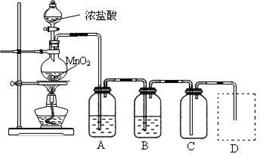
写出A、B中所盛放最佳化学试剂的名称 、 ,画出虚线框内所需装置图并标明所需试剂的名称。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②: ;假设③: 。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 | | 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |
(18分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气
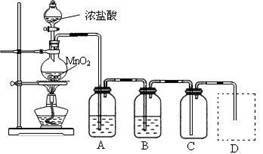
写出A、B中所盛放最佳化学试剂的名称 、 ,画出虚线框内所需装置图并标明所需试剂的名称。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②: ;假设③: 。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
|
实验方法 |
实验现象 |
结论 |
|
在溶液中加 KSCN溶液 |
|
固体物质中有FeCl3 |
|
向a溶液中滴加 酸性KMnO4溶液 |
KMnO4溶液紫色 不褪色 |
固体物质中不含______ |
由此得出结论:假设 成立(填序号①②③)。
Ⅲ、为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2]
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
IV、a溶液常作印刷电路铜板的腐蚀剂,写出发生反应的离子方程式 。活动小组的同学们又设计了两种从上述废液中回收Cu的方案:
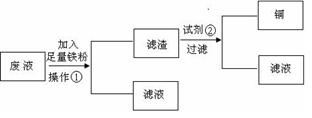
方案1:设计流程图如下:
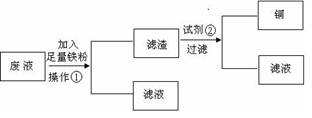
请分别写出操作①和试剂②的名称_________,_______。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,铜作________极。当观察到阴极有少量气泡产生时,停止电解,这时要回收的Cu已全部析出。
评价:方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为: 。
一、1.AD 2.B 3.B 4.D 5.D 6.BC 7.C 8.A?
二、9.C4H10,C9H20或C10H8?
10.(1)CO、H2,物质的量相同,耗O2的量相同?
(2)C2H5OH,CH3―O―CH3,必须是同分异构体?
11.(1)CH≡CH,有机物分子式和结构式的确定.files/image071.jpg) ,(2)CH4,CH3OH
,(2)CH4,CH3OH
12.C5H12;设该烃的分子式为CxHy,则有有机物分子式和结构式的确定.files/image073.gif) =5/1则x/y=5/12所以分子式为C5H12
=5/1则x/y=5/12所以分子式为C5H12
13.(1)x=2,y=1 (2)C2H2O2 (3)18
14.(1)1≤V(O2)/V(C2H6)≤2.5?
当只有CO2与Na2O2反应时,则应通入的O2最多,由2C2H6+5O2+4Na2O2→4Na2CO3+6H2O(l)得V(O2)/V(C2H6)=5/2=2.5?
当C2H6燃烧后产生的CO2和H2O均全部与Na2O2反应时,则通入的O2应最少,由方程式C2H6+O2+5Na2O2→2Na2CO3+6NaOH得V(O2)/V(C2H6)=1/1
故O2与C2H6的体积比x的取值范围为1≤V(O2)/V(C2H6)≤2.5
(2)0.8?
n(Na2O2)=有机物分子式和结构式的确定.files/image075.gif) =0.02mol由
=0.02mol由
有机物分子式和结构式的确定.files/image077.gif) =
=有机物分子式和结构式的确定.files/image079.gif)
有机物分子式和结构式的确定.files/image081.gif) n(O2)=0.025mol故通入O2的质量不能超过
n(O2)=0.025mol故通入O2的质量不能超过
15.(1)n(H2O)=有机物分子式和结构式的确定.files/image083.gif) =0.6moln(CO2)=
=0.6moln(CO2)=有机物分子式和结构式的确定.files/image085.gif) =0.4mol?
=0.4mol?
CuO + CO = Cu + CO2 △m(减量)?
1mol
1mol
n(CO)
有机物分子式和结构式的确定.files/image081.gif)
有机物分子式和结构式的确定.files/image087.gif)
∴实际有机物燃烧产生的CO2为:0.4-0.2=0.2mol?
∴0.2mol有机物中含有机物分子式和结构式的确定.files/image087.gif)
有机物分子式和结构式的确定.files/image081.gif) 1mol有机物中C∶H∶O=2∶6∶2
1mol有机物中C∶H∶O=2∶6∶2
故有机物分子式为:C2H6O2?
(2)n(Na)=有机物分子式和结构式的确定.files/image090.gif) =0.4mol,0.2mol有机物能和0.4molNa反应
=0.4mol,0.2mol有机物能和0.4molNa反应
所以该有机物为二元醇,结构简式为HO―CH2―CH2―OH?
16.(1)有机物分子式和结构式的确定.files/image092.jpg)
2-甲基-1,3-丁二烯(或异戊二烯)?
(2)有机物分子式和结构式的确定.files/image094.jpg) ?聚异戊二烯?
?聚异戊二烯?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com