2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO
2的含量及有效地开发利用CO
2,引起了全世界的普遍重视.为减小和消除CO
2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO
2创新利用的研究.
(1)目前工业上有一种方法是用CO
2来生产燃料甲醇.为探究该反应原理,进行如下实验:
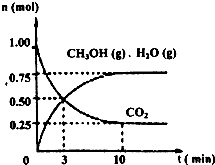
某温度下,在容积为2L的密闭容器中,充入1mol CO
2和3.25mol H
2,在一定条件下发生反应,测得CO
2、CH
3OH(g)和H
2O(g)的物质的量(n)随时间变化如右图所示:
①从反应开始到平衡,氢气的平均反应速率v(H
2)=
0.1125mol/(L?min)
0.1125mol/(L?min)
.
②下列措施中一定不能使n(CH
3OH)/n(CO
2)增大的是:
D
D
.
A.降低温度 B.缩小容器的容积 C.将水蒸气从体系中分离 D.使用更有效的催化剂
(2)常温常压下,饱和CO
2水溶液的pH=5.6,c(H
2CO
3)=1.5×l0
-5mol?L
-1.若忽略水的电离及H
2CO
3的第二级电离,则H
2CO
3?HCO
3-+H
+的电离平衡常数K=
4.2×10-7
4.2×10-7
.(已知:10
-5.6=2.5×l0
-6).
(3)标准状况下,将1.12LCO
2通入100mL 1mol?L
-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序为
c(Na+)>c(CO2-3)>c(OH-)>c(HCO-3)>c(H+)
c(Na+)>c(CO2-3)>c(OH-)>c(HCO-3)>c(H+)
;
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示
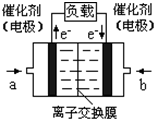
意图,则a处通入的是
乙醇
乙醇
(填“乙醇”或“氧气”),
b处电极上发生的电极反应是:
O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
.
(5)CO
2在自然界循环时可与CaCO
3反应,CaCO
3是一种难溶物质,其Ksp=2.8×10
-9.CaCl
2溶液与Na
2CO
3溶液混合可形成CaCO
3沉淀,现将等体积的CaCl
2溶液与Na
2CO
3溶液混合,若Na
2CO
3溶液的浓度为2×10
-4mol/L,则生成沉淀所需CaCl
2溶液的最小浓度为
5.6×10-5mol/L
5.6×10-5mol/L
.

 2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
2009年12月7日一18日在丹麦首都哥本哈根召开的联合国气候会议,就未来应对气候变化的全球行动签署新的协议.而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究. 意图,则a处通入的是
意图,则a处通入的是