
题目列表(包括答案和解析)

①按图装配实验装置。
②洗净试管然后充分干燥。
③向连接500 mL烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶、烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管里的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置放置冷却到室温。
⑧调节烧杯的高度使烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
根据上述实验,完成下列问题。
(1)在操作①中,装置冷却后,玻璃管C的出口,一直要在烧杯的水中,不能离开水面,其理由是__________________________________。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度使烧杯中的水与烧瓶中的水面一致?
答:__________________________________________。
(3)标准状况下,1 mol氧气所占的体积(保留小数点后两位)为____________L;混合物中MnO2的质量分数为____________。

①按如图连接实验装置并检验气密性。
②洗净试管然后充分干燥。
③向500 mL烧瓶里装满水,向500 mL烧杯里加少量水,把连接烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管质量为14.5 g,往试管里加入KClO3和MnO2的混合物,称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶和烧杯中的水面一致,再关闭弹簧夹然后把杯中的水倒掉。
⑥加热试管的混合物到不再产生气体,而且水不再向烧杯中流为止。
⑦反应完毕后把装置放置冷却到室温。
⑧调节烧杯的高度使烧瓶和烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 L量筒测量烧杯里水的体积为285.0 mL,换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后的试管的质量为15.55 g。
根据上述实验,完成下列问题:
(1)在操作⑦中,装置冷却时,玻璃管C的出口一定要在烧杯的水中,不能离开水面,其理由是__________________。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致?__________________。
(3)计算标准状况下,1 mol氧气所占的体积(保留小数点后两位)_________ L。
(10分)一定量的液态化合物![]() ,在一定量的
,在一定量的![]() 中恰好完全燃烧,反应方程式为
中恰好完全燃烧,反应方程式为![]() ,冷却后,在标准状况下测得生成物的体积是672mL,密度是
,冷却后,在标准状况下测得生成物的体积是672mL,密度是![]() 。则:
。则:
(1)反应前![]() 的体积是 mL。
的体积是 mL。
(2)化合物![]() 的摩尔质量是 。(用含
的摩尔质量是 。(用含![]() 的代数式表示)。
的代数式表示)。
(3)若![]() 分子中X、Y两元素的质量比是3 :16,且
分子中X、Y两元素的质量比是3 :16,且![]() ,则X、Y两元素分别为 和 (写元素符号)。
,则X、Y两元素分别为 和 (写元素符号)。
一定量的液态化合物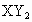 ,在一定量的氧气中恰好完全燃烧,反应的方程式为:
,在一定量的氧气中恰好完全燃烧,反应的方程式为: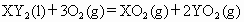
冷却后,在标准状况下测得生成物的体积为672mL,密度为2.56g/L.
(1)反应前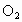 的体积是__________mL(STP).
的体积是__________mL(STP).
(2)化合物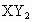 的摩尔质量是__________.
的摩尔质量是__________.
(3)若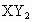 分子中X、Y两元素的质量比为3∶16,则X、Y两元素的符号分别是________和________.
分子中X、Y两元素的质量比为3∶16,则X、Y两元素的符号分别是________和________.
一定量的液态化合物 ,在一定量的氧气中恰好完全燃烧,反应的方程式为:
,在一定量的氧气中恰好完全燃烧,反应的方程式为: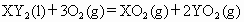
冷却后,在标准状况下测得生成物的体积为672mL,密度为2.56g/L.
(1)反应前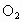 的体积是__________mL(STP).
的体积是__________mL(STP).
(2)化合物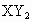 的摩尔质量是__________.
的摩尔质量是__________.
(3)若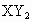 分子中X、Y两元素的质量比为3∶16,则X、Y两元素的符号分别是________和________.
分子中X、Y两元素的质量比为3∶16,则X、Y两元素的符号分别是________和________.
一、1.BD 2.AD 3.A?
4.解析:2CO+O2 2CO2 ΔV
2CO2 ΔV
2 1 2 1
50 mL
若O2过量:V(CO)=100 mL;若CO过量:V(O2)=50 mL则V(CO)=150 mL。
答案:AB?

则CO%=50%。
答案:A
6.D 7.B 8.D 9.A?
二、10.(1)V(CO)=2(m-n)L V(O2)=(2n-m)L V(CO)=n L
V(O2)=(m-n)L?
(2)CO2、CO
11.BD
12.(1)672 mL (2)76 g?mol-1?
13.N2O NO 1∶4?
14.(1)t℃、p Pa时D的密度a g?L-1?
m(C)=30.5 g-a g?L-1×3 L=(30.5-3 a)g?
(2)盐酸的浓度b mol?L-1?
若Mg过量,V(H2)= ×22.4 L?mol-1
×22.4 L?mol-1
若HCl过量:
V(H2)= ×22.4 L?mol-1?
×22.4 L?mol-1?
若正好完全反应,V(H2)上述两值等效,均可。?
15.(1)4∶3 (2)0.91 g/L?
16.(1)1 固体的量增加,产生气体的量增加,说明在1中有酸剩余。?
(2)固体为Na2CO3和NaHCO3的混合物:
Na2CO3%=55.79% NaHCO3%=44.21%?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com