
题目列表(包括答案和解析)
| NO | - 3 |
现有两份体积相同的混合溶液,其组成如下:
|
|
KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
|
(1) |
0.4 mol |
0.1mol |
0.3mol |
0.1mol |
|
(2) |
0.2mol |
0.2mol |
0.1mol |
0.1mol |
则两份溶液中各离子浓度( )
A. 仅c(K+)相同 B. 仅c(Cl-)相同 C. 完全相同 D. 完全不同
Ⅰ⑴玻璃棒是中学化学实验中常用的仪器。下列过程中,一般不需要玻璃棒的是 ( 填写编号 )
①用PH试纸测定Na2CO3溶液的PH
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化。
⑤实验室用新制备的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
⑵用“大于”“等于”“小于”填空
① 读量筒中液体的体积时,视线偏高,读取的体积数 实际体积数
② 用托盘天平称取10.4g食盐,将砝码和食盐的位置颠倒,所称食盐的质
量 10.4g
③配制500ml 0.1mol/lNaOH溶液,定容时俯视刻度线,所得溶液的物质的量浓
度 0.1mol/l
④用中和滴定法测某NaOH溶液的浓度,量取待测液未用该溶液润洗滴定管,测得的溶液的浓度 实际浓度
Ⅱ、氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:![]()
![]()
![]() 、
、![]() 、
、![]() 、
、![]()
![]() 四种物质中的一种物质能使上述还原过程发生。
四种物质中的一种物质能使上述还原过程发生。
(1)写出该氧化还原反应的方程式(不配平): 。
(2)该反应中氧化剂和还原剂物质的量之比为 。
(3)反应中硝酸体现了 、 性质。
(4)反应中若产生0.1mol气体,则转移电子的物质的量是 。
| B | ||
| A | X | C |
| D |
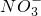 +10H++8e-→N2O+5H2O
+10H++8e-→N2O+5H2O +10H++8e-→N2O+5H2O
+10H++8e-→N2O+5H2O一、1.解析:设原溶液中水的质量为w g,R的质量为 m g,R的溶解度为S g,则有:

根据比例性质,可设:?

S= ×100=
×100=
答案:B?
2.解析:注意体积效应。?
答案:B?
3.解析:因H2SO4溶液的密度随浓度增大而增大,是一个变值而不是一个定值。设稀释后溶液密度为ρ′,则有:18× ×10-3=9×
×10-3=9× ×10-3,2
×10-3,2 =
= ,因为
,因为
ρ′<ρ,故V<100(mL)。
答案:A?
4.解析:NH3+2O2===HNO3+H2O?
HNO3%= ×100%=78%
×100%=78%
答案:A
5.AB 6.B 7.B 8.D 9.C?
二、10.
11.
 g
g
12.(1)G、E、C、H、F(或E、G、C、H、F)?
(2)BCD
14.(1)0.0813 mol?L-1 (2)32 mL?
15.(1)四种?
①KOH,K2CO3 ②K2CO3 ③K2CO3,KHCO3?④KHCO3?
(2)解:2KOH+CO2 === K2CO3+H2O?
22.4 138?
2.24 x=13.8?
KOH+CO2===KHCO3?
22.4 100?
2.24 x=10.0?
从上面两方程知:生成的固体全部是K2CO3时应该是 =0.100 mol
=0.100 mol
若K2CO3为a mol,则KHCO3为(0.100-a)mol?
则得方程
即K2CO3和KHCO3各为0.050 mol?
K2CO3为:
KHCO3为:
依K+守恒的要求,设KOH溶液浓度为c则:?
0.300 Lc=0.050 mol×2+0.050 mol c=0.50 mol?L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com