
题目列表(包括答案和解析)
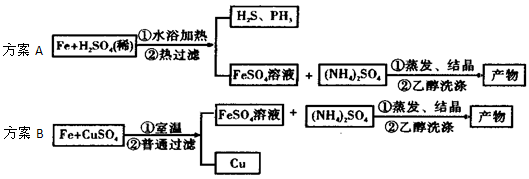
探究一:该小组制备溴乙烷的主要步骤如下:?
①向装置图所示的U形管和大烧杯中加入冷水;?
②在小烧杯中按一定比例配制乙醇、水、浓硫酸混合液;?
③向装置图所示的圆底烧瓶中加入一定量研细的溴化钠和少量碎瓷片;?
④将冷却至室温的混合液转移到圆底烧瓶中,加热;
⑤精制溴乙烷。?

回答下列问题:?
(1)步骤②向乙醇和水缓缓加入浓硫酸时,小烧杯要置于冷水中冷却,除了避免硫酸小液滴飞溅外,更主要的目的是___________________。?
(2)步骤④加热片刻后,烧瓶内的混合物会出现橘红色,出现这种现象的原因是(请用化学方程式表示)_____________________________,改用小火加热后,橘红颜色会逐渐消去,消失的原因是(请用化学方程式表示)__________________________________。?
(3)为了更好地控制反应温度,除按图示小火加热,还可采用的加热方式是________________。
(4)步骤⑤反应结束后,将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,弃去(填“上层”或“下层”)_________液体。为了除去粗产品中的杂质,可用下列试剂中的________(填序号)。
A.氢氧化钠稀溶液
B.碳酸钠稀溶液?
C.硝酸银溶液
D.四氯化碳?
探究二:溴乙烷与NaOH乙醇溶液的反应?
学习小组在进行溴乙烷与NaOH乙醇溶液的反应中,观察到有气体生成。?
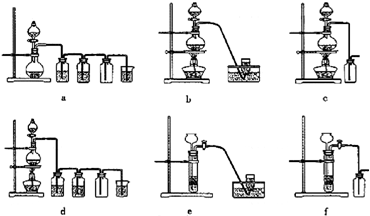
请你设计两种不同的方法分别检验该气体,并使用下列简易图标,在答题卡的方框中画出这两种方法的实验装置示意图(所给各种图标,使用次数不限,也可以不全部用),并写出装置中所盛试剂的名称(试剂任选)和实验现象。?


(15分)
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
NaBr+H2SO4 HBr+NaHSO4
HBr+NaHSO4
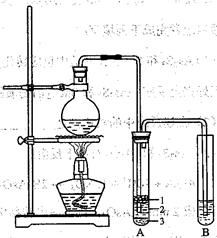
CH3CH2OH+HBr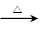 CH3CH2Br+H2O
CH3CH2Br+H2O
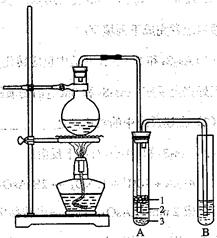
化学兴趣小组根据实验原理设计如右图的装置。
根据题意完成下列填空:有关数据列表如下:
| | 乙醇 | 溴乙烷 |
| 状态 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.8 | 1.4 |
| 沸点/℃ | 78.5 | 119.0 |
| 熔点/℃ | -l30 | 38.4 |
 HBr+NaHSO4
HBr+NaHSO4 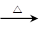 CH3CH2Br+H2O
CH3CH2Br+H2O| | 乙醇 | 溴乙烷 |
| 状态 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.8 | 1.4 |
| 沸点/℃ | 78.5 | 119.0 |
| 熔点/℃ | -l30 | 38.4 |


| ||
| ||
| △ |
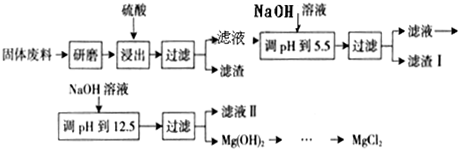
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com