
题目列表(包括答案和解析)
200°C时,11.6克C02和水蒸气的混合气体与足量的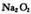 充分反应后,固体的质量增加了 3. 6克。从以上信息中,我们得出的下列结论中不正确的是
充分反应后,固体的质量增加了 3. 6克。从以上信息中,我们得出的下列结论中不正确的是
A. 可以计算出混合气体中CO2和水蒸气的质量
B. 可以判断出混合气体的平均摩尔质量
C. 可以计算出该反应中转移的电子数
D. 可以总结出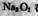 t任何反应中既作氧化剂也作还原剂
t任何反应中既作氧化剂也作还原剂
200°C时,11.6克C02和水蒸气的混合气体与足量的Na2O2充分反应后,固体的质量增加了 3. 6克。从以上信息中,我们得出的下列结论中不正确的是
| A.可以计算出混合气体中CO2和水蒸气的质量 |
| B.可以判断出混合气体的平均摩尔质量 |
| C.可以计算出该反应中转移的电子数 |
| D.可以总结出Na2O2任何反应中既作氧化剂也作还原剂 |
200°C时,11.6克C02和水蒸气的混合气体与足量的充分反应后,固体的质量增加了 3. 6克。从以上信息中,我们得出的下列结论中不正确的是
A. 可以计算出混合气体中CO2和水蒸气的质量
B. 可以判断出混合气体的平均摩尔质量
C. 可以计算出该反应中转移的电子数
D. 可以总结出t任何反应中既作氧化剂也作还原剂
合成氨工业用氢和氮在催化剂作用下直接合成,下表表示在一定温度和压强作用下达到动态平稳时氨的含量。
达到平稳时混合气体中氨的含量(体积百分比)(氮气和氢气的体积比是1:3)
|
t(℃) | 100 | 200 | 300 | 600 | 1000 |
| 200 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
|
总体积为44.8L,现将400℃、300大气压的氢气33.6L和400℃、
300大气压的氮气11.2L充入容器中,当两者反应达到动态平稳
时,若保持混合气体的温度和压强仍为400℃和300大气压,求:
(1)容器是向外界放热,还是吸热?为什么?
(2)试计算充入容器中氮气质量是多少克?
(3)活塞C要向左侧移动的距离与容器全长之比是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com