
题目列表(包括答案和解析)
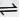 H2SO3、2H2SO3+O2═2H2SO4
H2SO3、2H2SO3+O2═2H2SO4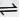 H2SO3、2H2SO3+O2═2H2SO4
H2SO3、2H2SO3+O2═2H2SO4下图表示常见元素单质及化合物相应转化关系,部分反应的产物没有全部列出。
已知:B是一种黄绿色气体,C在所有气体中密度最小,D是一种碱;X、Y是生活中应用最为广泛的金属,F是一种红棕色氧化物,常用作红色油漆和涂料;Z为气态氧化物。
请回答下列问题:
(1)气体B具有 (填“还原性”、“氧化性”或“漂白性”),反应②属于四种基本反应类型反应中的 。
(2) 有学生认为B与X反应的产物E不一定是纯净物。他认为产物中可能还有 (填化学式),为验证其猜想该同学设计了相关实验,你认为他需要选择的试剂为 (填序号)。
a.酸性高锰酸钾溶液 b.NaOH溶液 c.KSCN溶液 d.稀硫酸
(3)若Z能导致温室效应,则反应③的离子反应方程式为 。
(4)若Z是我国酸雨形成的罪魁祸首,目前应用最广泛的工业处理含Z废气的方法是在一定条件下与生石灰作用而使其固定,产物可作建筑材料,反应的化学方程式为 。
(5)若Z是形成酸雨的另一种主要物质,Z与足量的D溶液反应时能被完全吸收,且生成两种盐(物质的量之比为1:1),请写出该反应的化学反应方程式 。
1
2
3
4
5
6
7
8
9
10
C
B
A
A
D
B
D
D
C
B
11
12
13
14
15
16
17
18
19
20
B
B
AC
D
A
A
C
A
A
C
21. NO2 SO2 机动车尾气
22.2SO2 + O2 2SO3 SO3 + H2 O H2 SO 4
23.盐析 还原性
24.简要回答下列问题.
(1)居室装修完毕,要通风才能入住,其原因是: 装修材料中含有对人体有害的挥发性物质,必须先除去
(2)可用铁罐盛装浓硫酸的原因是:常温铁在浓硫酸中会形成致密坚固的氧化膜
(3)胃舒平(主要成分Al(OH)3)治疗胃酸过多的原理(用离子方程式表示):
Al(OH)3+3H+=Al3++3H2O
(4)碳酸氢钠产生疏松作用的原理:(用化学方程式表示)
2NaHCO3Na2CO3+H2O+CO2↑
25.① 甲 使蛋白质水解生成对人体有益的氨基酸
② 乙 氨基酸氧化酶具有专一性不能使蛋白质水解而清除
26、(1)( D )(2)过滤用到的三种玻璃仪器主要有 玻璃棒、漏斗、烧杯 .
(3) 萃取 . 水层 .
(4) ( BC )A.酒精 B.汽油 C.苯
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com