
题目列表(包括答案和解析)
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键能之和的差。
|
化学键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1mol化学键时放出的能量 |
436kJ |
243kJ |
431kJ |
则下列化学方程式不正确的是
A.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=-91.5kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g);△H=-183kJ·mol-1
C.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=+91.5kJ·mol-1
D.2HCl(g) =H2(g)+Cl2(g) ;△H=+183kJ·mol-1
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键能之和的差。
| 化学键 | H-H | Cl-Cl | H-Cl |
| 生成1mol化学键时放出的能量 | 436kJ | 243kJ | 431kJ |
则下列化学方程式不正确的是
A.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=-91.5kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g);△H=-183kJ·mol-1
C.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=+91.5kJ·mol-1
D.2HCl(g) =H2(g)+Cl2(g) ;△H=+183kJ·mol-1
|
从手册上查得:H-H、Cl-Cl和H-Cl的键能分别为436、243和431kJ/mol.请用此数据估计由Cl2、H2反应生成1molHCl时的热效应: | |
| [ ] | |
A. |
放热183kJ |
B. |
放热91.5kJ |
C. |
吸热183kJ |
D. |
吸热91.5kJ |
如图所示是101kPa时,氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )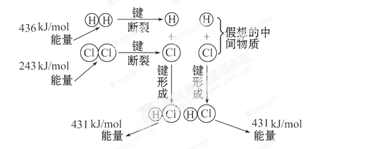
| A.此反应的热化学方程式为:H2(g)+Cl2(g) =2HCl(g) ΔH=+183kJ·mol-1 |
| B.2molHCl分子中的化学键形成时要释放862kJ能量 |
| C.1molH2中的化学键断裂时需要吸收436kJ能量 |
| D.此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g) =HCl(g) ΔH=-91.5kJ·mol-1 |

| A.此反应的热化学方程式为:H2(g)+Cl2(g) =2HCl(g) ΔH=+183kJ·mol-1 |
| B.2molHCl分子中的化学键形成时要释放862kJ能量 |
| C.1molH2中的化学键断裂时需要吸收436kJ能量 |
| D.此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g) =HCl(g) ΔH=-91.5kJ·mol-1 |

Cu是正极,正极反应式:2Fe3++ 2e?= 2 Fe2+
Fe是负极,负极反应式:Fe ?2e?= Fe2+
e? I
Fe Cu
|