
题目列表(包括答案和解析)



 【物质结构与性质】
【物质结构与性质】| m | n |
【物质结构与性质】(8分)
组成蛋白质的元素主要有C、H、O、N及S、P和少量的Cu、Fe、Zn等,其中铜及其合金是人类最早使用的金属材料,用途广泛。
(1)铜原子的核外电子排布式是 ;O、N、S的第一电离能由大到小的顺序为 。
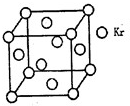
(2)铜的熔点比钙高,其原因是 ;
右图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为 。
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有 (填序号)。
A.配位键B.金属键C.极性共价键D.非极性共价键E.离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 (填序号)。
A.平面正方形 B.正四面体 C.三角锥型 D.V型
③某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:
HOCH2CH=CH2→CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化方式为 。
【物质结构与性质】
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)(2分)CH3+、·CH3、CH3-都是重要的有机反应中间体,有关它们的说法正确的是
A.它们均由甲烷去掉一个氢原子所得
B.它们的空间构型相同,碳原子均可以采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp3杂化,所有原子均共面
(2)(3分)在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
①HCl、CS2、H2S、SO2四种分子中μ=0的是 ;
②实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是 构型,BCl3分子是 构型。
(3)(2分)对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。
(4)(3分)利用光电子能谱证实:在洁净铁(可用于合成氨
反应的催化剂)的表面上存在氮原子,右图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在单层晶面上N/Fe原子数之比为________________。

(5)(2分)金属晶体的结构可用等径圆球的密堆积来描述,在等径圆球的最密堆积的各种形式中,立方最密堆积和六方最密堆积最为重要,请指出下图中哪个为立方最密堆积 (填“A”或“B”)
图A 图B
1、B 2、C 3、、C 4、A 5C 6、B 7、C 8、D 9、B 10、BC 11、C 12、BD 13、AC 14、B的
15.题答案:(10分)(每空2分)
(I)(1)10600n/197m% (2)沿玻璃棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次 (3)① 加入BaCl2溶液,生成的沉淀质量大,测量的相对误差小;②过量的Ca2+可与OH-生成微溶的Ca(OH)2沉淀影响测定结果
(II)(1)4 (2)① 装置中原有空气中的CO2没有排出,最终也被碱石灰吸收 ②反应完成后,装置中的CO2没有全部被碱石灰吸收 ③空气中的CO2和水蒸气被碱石灰吸收
16.16(12分)
(1)Al2O3 + Na2CO32NaAlO2 +CO2↑;(2分)
(2)NaFeO2 + 2H2O = Fe(OH)3↓ + NaOH(2分)。
(3)由于溶液在硅酸钠和偏铝酸钠发生水解,降低pH值有利于水解平衡向正反应方向移动,当pH调到7~8时,使它们水解完全,从而除去SiO32-和AlO2-。(共2分)
(4)2CrO42-+2H+ Cr2O72-+H2O(2分)
(5)①当滴加最后一滴硫代硫酸钠溶液,溶液蓝色褪去,半分钟内不复现(2分)
②94.08%(2分)。
17、(共10分)
(1)HNO3 Ag (每空1分)
(2)氧气 氢氧化铜悬浊液(或其他合理答案) (每空2分)
(3)①4Ag++2H2O = 4Ag↓+4H++O2↑ (2分)
②HCHO+2Ag(NH3)2++2OH- HCOO-+NH4++2Ag↓+3NH3+H2O (2分)
18.(8分)
(1)BD(2分)
(2)C (1分)该反应达到平衡时,平衡常数K=,增大容器体积时,c(CH3OH)和c(CO)等比例减小,由于H2浓度不变,此时的值仍然等于K,所以平衡不移动。(1分)
(3)越高(1分)
原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高碳转化率又降低且有甲烷生成。(1分)
(4)温度 压强 CO和H2的体积分数之比 (2分)
19、(共12分)
(1) 取代(或水解) 消去(每空1分)
(2) (2分)
(3)+ NaOH
(4)(2分,对1 个即可)
(5)(4分。到(CH2=CH)2CuLi给2分,到苯乙烯给3分,到聚苯乙烯给4 分,漏条件整体扣1 分)
20.(共8分)(1)由题意知(C6H10O5)n+nH2O 3nCH4↑+3nCO2↑
162n 3n
(2)要保证CO和H2的充分利用,则只能是生成的CO和H2必须是1:2。在100m3的天然气中有CH495m3和CO25m3。解设通入的水蒸气为Xm3,则有
CH4+CO2→2H2+2CO CH4+H2O→3H2+CO
5 5 10 10 X X 3X X
2CH4 + O2→ 4H2 + 2CO
95-5-X 2(95-5-X) 95-5-X
所以有,可以得出X=10(m3),
(3)80.5t
21.(共12分)
(1)平面正三角形(1分) N>S>Si(1分)
(2)N2O4(1分) 第四周期ⅤA(1分) 3d54s2(1分)
(3) N2,CO,C22-,CN-(4个中任选3个,每个1分) 1(0.5分) 2(0.5分)
(4)4(1分) 8(1分) 8(0.5分) 16(0.5分)
解析:(1) SiO32-、SO32-、NO3-三种离子中中心原子的杂化类型均为sp2杂化,离子构型为平面正角形,键角为120°(3)π键和σ键共存在,多重键中只有一个是σ键,其余均为π键,如双键中有1个σ键和1个π键,叁键中有1个σ键和2个π键。(4)PO43-中P原子以4个sp3杂化轨道和4个O原子成键,所以P为4配位氧。根据题意可先计算出Si晶胞中Si原子数:8×+6×+4=8(个),SiO2晶胞中Si原子数目与硅晶胞中Si原子数目相同,再可结合SiO2晶体中硅氧原子数目1:2的特点可确定晶胞中O原子数有16个(对题中描述的复杂结构可视为干扰条件)。
21B.答案:(1) MnO2 + 4H+ + 2Cl- = Mn2+ + Cl2 + 2H2O (1分)
(2) 假设一 氯气使布条褪色 假设二 HClO使布条褪色 假设三 盐酸使布条褪色
实验①:把红色干布条放入充满氯气的集气瓶中,布条不褪色;
实验②把红色布条伸入稀盐酸中,红色布条不褪色 (每空1分)
结论:次氯酸使布条褪色 (1分)
(3) 下层液(1分) 上层液 (1分)
(4)会造成环境污染 (1分) (或其它合理答案) (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com