
题目列表(包括答案和解析)
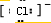
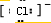
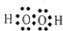
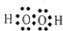
| ||
| ||
化合物H是重要的有机化合物,可由E和F在一定条件下合成:(有些反应条件省略如:加热等)
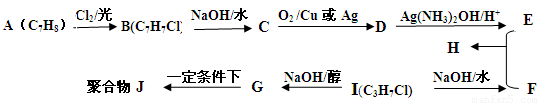
已知以下信息:
A属于芳香烃,H属于酯类化合物。
I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)B的结构简式 ,C的官能团名称 。
(2)B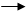 C;G
C;G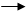 J两步的反应类型 ,
。
J两步的反应类型 ,
。
(3)①
E+F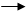 H的化学方程式
。
H的化学方程式
。
②I G 的化学方程式
。
G 的化学方程式
。
(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①属于芳香族化合物
②能和饱和NaHCO3溶液反应放出CO2,共有______种(不考虑立体异构)。
K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式 。
已知A、B、C、D四种短周期元素,它们的核电荷数A<B<C<D。其中A、B、C是同一周期的非金属元素。化合物DC为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。下列说法正确的是
A.A、B、C的氢化物的沸点逐渐降低
B.最高价氧化物的水化物的酸性A>B
C.单质D与AC2可以发生置换反应得到DC
D.B与C只能形成BC和BC2两种化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com