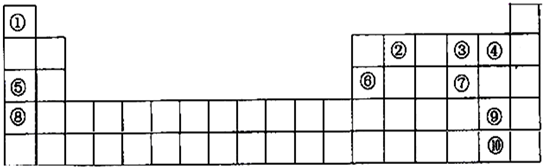
下列框图中的每一个字母都是中学化学中常见的物质,所有物质均由短周期元素组成,其中B、C、G、K、L都含有同一种元素.B、E、F、I为单质.常温常压下D为液体,E、F、I为气体,F是空气的主要成分之一.C由两种元素组成,其晶体熔点高、硬度大,闪烁着晶莹的光泽.这些物质之间有可能发生如下转化,其反应关系如图所示:

(1)写出A的电子式
,B的原子结构示意图
,D的结构式是
H-O-H
H-O-H
E在I中燃烧的现象为
苍白色火焰(产生白雾)
苍白色火焰(产生白雾)
.
(2)25°C,101kPa下,2gE完全燃烧放出285.8kJ的热量,写出E+F→D的热化学反应方程式
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1
.
(3)铂做电极E与F、KOH溶液构成原电池,其负极反应为
H2-2e-+2OH-=2H2O
H2-2e-+2OH-=2H2O
;如果将通入的E改成CH
4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH
4+2O
2+2KOH=K
2CO
3+3H
2O,则该电池的负极反应式为:
CH4+10OH--8e-=CO32-+7H2O
CH4+10OH--8e-=CO32-+7H2O
.
(4)如图所示,A与C两种固体混合后,加入液体D,可能发生反应的化学方程式为
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
,
Al2O3+2NaOH=2NaAlO2+H2O
Al2O3+2NaOH=2NaAlO2+H2O
.
(5)K+G═L的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.







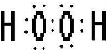
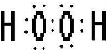
 A、B、C是由H、O、Na三种元素中的两种或三种元素组成的三种化合物,其中化合物A为淡黄色固体.甲、乙、丙是三种单质,分别由上述元素组成.上述单质和化合物之间存在如图反应关系:
A、B、C是由H、O、Na三种元素中的两种或三种元素组成的三种化合物,其中化合物A为淡黄色固体.甲、乙、丙是三种单质,分别由上述元素组成.上述单质和化合物之间存在如图反应关系: