
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
КЃЫЎжажївЊРызгЕФКЌСПШчЯТЃК
|
ГЩЗж |
КЌСП/(mg/L) |
ГЩЗж |
КЌСП/(mg/L) |
|
Cl- |
18980 |
Ca2+ |
400 |
|
Na+ |
10560 |
HCO3- |
142 |
|
SO42- |
2560 |
Mg2+ |
1272 |
ЃЈ1ЃЉГЃЮТЯТЃЌКЃЫЎЕФpHдк7.5~8.6жЎМфЃЌЦфдвђЪЧ(гУРызгЗНГЬЪНБэЪО)______________________________ЁЃ
ЃЈ2ЃЉЕчЩјЮіЗЈЕЛЏКЃЫЎЪОвтЭМШчЭМЫљЪОЃЌЦфжавѕ(бє)РызгНЛЛЛФЄНідЪаэвѕ(бє)РызгЭЈЙ§ЁЃвѕМЋЩЯВњЩњЧтЦјЃЌвѕМЋИННќЛЙВњЩњЩйСПАзЩЋГСЕэЃЌЦфГЩЗжга________КЭCaCO3ЃЌЩњГЩCaCO3ЕФРызгЗНГЬЪНЪЧ_______________ЁЃ

ЃЈ3ЃЉгУКЃЫЎПЩЭЌЪБЩњВњТШЛЏФЦКЭН№ЪєУОЛђУОЕФЛЏКЯЮяЃЌЦфСїГЬШчЯТЭМЫљЪОЃК
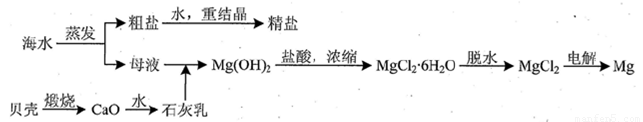
ЂйдкЪЕбщЪвжагЩДжбЮЁАжиНсОЇЁБжЦОЋбЮЕФВйзїАќРЈШмНтЁЂЙ§ТЫЁЂеєЗЂЁЯДЕгЕШВНжшЃЛгаЙиЦфжаЁАеєЗЂЁБВНжшЕФа№Ъіе§ШЗЕФЪЧ_____ЁЃ
aЃЎеєЗЂЕФФПЕФЪЧЕУЕНШШБЅКЭШмвК
bЃЎеєЗЂЕФФПЕФЪЧЮіГіОЇЬх
cЃЎгІгУгрШШеєИЩШмвК
dЃЎгІеєЗЂжСгаНЯЖрОЇЬхЮіГіЪБЮЊжЙ
ЂкгЩMgCl2ШмвКЕУЕНMgCl2•6H2OОЇЬхЪБЃЌвВашвЊеєЗЂЃЌеєЗЂЕФФПЕФЪЧЕУЕНШШБЅКЭШмвКЃЌХаЖЯШмвКвбБЅКЭЕФЯжЯѓЪЧ_________________________ЁЃ
ЃЈ4ЃЉ25ЁцЪБЃЌБЅКЭMg(OH)2ШмвКЕФХЈЖШЮЊ5ЁС10-4 molЃЏLЁЃ
ЂйБЅКЭMg(OH)2ШмвКжаЕЮМгЗгЬЊЃЌЯжЯѓЪЧ___________________________ЁЃ
ЂкФГбЇЯАаЁзщВтКЃЫЎжаMg2+КЌСП(mg/L)ЕФЗНЗЈЪЧЃКШЁвЛЖЈЬхЛ§ЕФКЃЫЎЃЌМгШызуСП_________ЃЌдйМгШызуСПNaOHЃЌНЋMg2+зЊЮЊMg(OH)2ЁЃ25ЁцЃЌИУЗНЗЈВтЕУЕФMg2+КЌСПгыБэжа1272mg/LЕФЁАецжЕЁББШЃЌЯрЖдЮѓВюдМЮЊ______ЃЅ[БЃСє2ЮЛаЁЪ§ЃЌКЃЫЎжаБЅКЭMg(OH)2ШмвКЕФУмЖШЖМвдl g/cm3МЦ]ЁЃ
КЃЫЎжажївЊРызгЕФКЌСПШчЯТЃК
| ГЩЗж | КЌСП/(mg/L) | ГЩЗж | КЌСП/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
| ГЩЗж | КЌСП/(mg/L) | ГЩЗж | КЌСП/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |

XЁЂYЁЂZЁЂWОљЮЊКЌга10ЕчзгЕФЮЂСЃЃЌWЮЊН№ЪєбєРызгЃЌXЁЂYЁЂZГЃЮТЯТЮЊЦјЬхЃЌ
ЃЈ1ЃЉвбжЊЃК W + X + H2O Ёњ АзЩЋГСЕэЁЃ
ЂйШєЪЕбщЪвгУЯТЭМЫљЪОзАжУЁЂИЩдяКЭЪеМЏзАжУжЦШЁВЂЪеМЏИЩдяЕФXЃЌAжаЗжвКТЉЖЗжаЕФвКЬЌЪдМСЕФвЧЦїЕФУћГЦЪЧ________ЃЌвЧЦїЕФСЌНгЫГађЮЊaЁњ________________________ЃЛ
ЂкгЩWРызгаЮГЩЕФПЩШмадбЮWClnЃЌЦфЫЎШмвКЯд_________адЃЌдвђЪЧ(гУРызгЗНГЬЪНБэЪО)_____________________________________________________
ЂлЮЊНјвЛВНШЗЖЈWЃЌНјааШчЯТЪЕбщЃЌЧыВЙШЋЪЕбщВйзїЁЂЯжЯѓКЭНсТлЃКШЁЩЯЪіАзЩЋГСЕэЩйСПжУгкЪдЙмжаЃЌ_____________________________________________________
ЃЈ2ЃЉГЃЮТЯТЃЌШЁ10 mL pH= aЕФYЕФЯЁШмвКЃЌМгЫЎЯЁЪЭЪБpHЫцШмвКЬхЛ§VЕФБфЛЏШчЭМЫљЪОЃЌдђЂйYЕФЛЏбЇЪНЮЊ__________ЁЃ
ЂкЯТСагаЙиYЕФа№Ъіе§ШЗЕФЪЧ__________
AЃЎYШмгкЫЎКѓВПЗжЗЂЩњЕчРы
BЃЎYЕФЫЎШмвКжаЕЮМгЪЏШяЪдвКЛсБфКь
CЃЎЯЁЪЭКѓШмвКжаЫљгаРызгЕФХЈЖШОљМѕаЁ
DЃЎЯЁЪЭКѓЃЌвѕРызгЕФЮяжЪЕФСПХЈЖШжЎКЭВЛБф
ЂлвЛЖЈСПXШмвККЭвЛЖЈСПЕФYЕФШмвКЛьКЯЃЌЫљЕУШмвКжаРызгХЈЖШЕФЕШЪНЙиЯЕЮЊЃК
ЃЈгУЪЕМЪРызгЗћКХБэЪОЃЉ
ЃЈ3ЃЉвбжЊH2ЕФШМЩеШШЮЊ285.8 kJЁЄmol-1ЁЃЯжгаZКЭH2 ЕФЛьКЯЦјЬхЙВ0.2 molЃЌгыO2ЭъШЋШМЩеЩњГЩH2O(l)КЭCO2(g)ЃЌзЊвЦЕчзгЕФЮяжЪЕФСПЮЊ1.0 molЃЌЗХГіЕФШШСПЮЊ117.6 kJЁЃаДГіZЭъШЋШМЩеЕФШШЛЏбЇЗДгІЗНГЬЪН__________________________________
ФГЛЏбЇаЫШЄаЁзщгУжЛКЌгаТСЁЂЬњЁЂЭЕФЙЄвЕЗЯСЯжЦШЁДПОЛЕФТШЛЏТСШмвКЁЂТЬЗЏОЇЬх(FeSO4ЁЄ7H2O)КЭЕЈЗЏОЇЬхЃЌвдЬНЫїЙЄвЕЗЯСЯЕФдйРћгУЁЃЦфЪЕбщЗНАИШчЯТЃК

ЃЈ1ЃЉаДГіКЯН№гыЩеМюШмвКЗДгІЕФРызгЗНГЬЪНЃК ЁЃ
ЃЈ2ЃЉгЩТЫвКAжЦAlCl3ШмвКЕФЭООЖгаЂйКЭЂкСНжжЃЌЭООЖЂкжаЭЈШыЕФФГЦјЬхЃЈЙЬЬЌЪБПЩгУгкШЫЙЄНЕгъЃЉЃЌаДГіИУЦјЬхЕФЕчзгЪН ЁЃФуШЯЮЊНЯКЯРэЕФЭООЖЪЧ ЃЈЬюЂйЛђЂкЃЉЃЌРэгЩЪЧЃК ЁЃ
ЃЈ3ЃЉТЫвКEШєЗХжУдкПеЦјжавЛЖЮЪБМфКѓЃЌШмвКжаЕФбєРызгГ§СЫ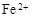 КЭ
КЭ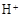 ЭтЃЌЛЙПЩФмДцдк
ЃЈгУРызгЗћКХБэЪОЃЉЃЌМьВтИУРызгЕФЗНЗЈЪЧ
ЁЃ
ЭтЃЌЛЙПЩФмДцдк
ЃЈгУРызгЗћКХБэЪОЃЉЃЌМьВтИУРызгЕФЗНЗЈЪЧ
ЁЃ
ЃЈ4ЃЉгУТЫдќFЭЈЙ§СНжжЭООЖжЦШЁЕЈЗЏЃЌгыЭООЖЂлЯрБШЃЌЭООЖЂмУїЯдОпгаЕФСНИігХЕуЪЧЃК ЁЂ ЁЃ
ЃЈ5ЃЉЭООЖЂмЗЂЩњЕФЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК ЁЃ
ЃЈ6ЃЉЪЕбщЪвДгCuSO4ШмвКжЦШЁЕЈЗЏЃЌВйзїВНжшгаеєЗЂХЈЫѕЁЂРфШДНсОЇЁЂ ЁЂздШЛИЩдяЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com