
题目列表(包括答案和解析)
(10分)感光高分子是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其他药品洗去。常用的感光高分子有某有机酸聚酯,它感光后形成二聚交联高分子,它的结构简式如下:
请据此回答下列问题:
(1)该有机酸聚酯可水解为两种分子,一种不含苯环的名称为________。另一种含苯环,其结构简式为__________。
(2)聚酯在光照下的二聚反应属_____反应(填反应类型)。
(3)乙炔与某有机酸在催化剂的作用下发生某种反应可获得该聚酯的单体,写出该反应方程式(有机物用结构简式表示):________________________。
(4)该聚酯水解得到的含羧基的有机物有多种同分异构体,其中含苯环且苯环上只有一个链状取代基并属于酯类的同分异构体,除
 外还有两种,请写出其结构简式:________、________。
外还有两种,请写出其结构简式:________、________。
( 10分 ) 下列6种有机物: A. 石蜡 B. 蔗糖?C. 甲苯 D. 甘油 E. 四氯化碳 F. 乙醛
( 1 ) 水解后产物能发生银镜反应的是 _____________ 。
( 2 ) 能用于制造炸药的是 _____________ 。
( 3 ) 能用作灭火剂的是 ___________ 。
( 4 ) 能从溴水中萃取溴的是 _______________ 。
( 5 ) 能溶解于水的是 ______________ 。
( 10分 ) 有机物A是一种含溴的酯,分子式为C6H9O2Br,已知有如下的转化关系:
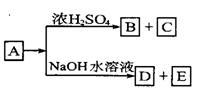
其中B、C含相同数目的碳原子,B既能使溴水褪色,又能跟Na2CO3溶液反应放出CO2气体,C依次进行氧化、消去反应后可以转化为B,经测定E是一种二元醇。
( 1 ) 写出结构简式: A _________ 、B __________ 、C __________ 、E _________ 。
( 2 ) 写出A在NaOH溶液中水解的化学方程式: _______________________________
10分)(1)现有0.1 mol·L-1的纯碱溶液,试用pH试纸测定溶液的pH,正确的操作是 __________。纯碱溶液呈碱性的原因(用离子方程式表式)是__________,你认为该溶液pH的范围一定介于__________之间。
(2)为探究纯碱溶液呈碱性是由![]() 引起的,请设计一个简单的实验方案。
引起的,请设计一个简单的实验方案。
( 10分) 甲、乙两池电极材料都是铁棒与碳棒(如下图)。请回答下列问题:

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的 棒;乙池中的 棒。
②在乙池中阳极的电极反应式是 。
(2)若两池中均盛放饱和NaCl溶液。
①写出乙池中发生总反应的离子方程式 。
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5:1,且生成两种酸。该反应的化学方程式为 。
③若乙池转移0.02mol电子后停止实验,池中溶液的体积是200mL,则溶液混匀后的pH= 。
一、选择题(1~10小题,每小题3分,共30分;11~20小题最多两个答案,每小题4分,答对一个得2分,答对两个得4分,但只要答错一个得0分)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
A
B
D
A
C
D
A
D
题号
11
12
13
14
15
16
17
18
19
20
答案
AD
A
D
D
BD
C
BC
AD
B
A
三、(共30分)
21、(7分)(1)CH3-O-CH2-OH CH2OH-CH2OH (各1分,共2分)
(2)(各1分,共2分。预期生成H2的体积与对应X的结构简式都对才得1分,只答对一部分不得分;体积没有单位合并扣1分,单位用毫升表示不扣分)
实验原理
预期生成H2的体积(标况)
对应X的结构简式
取
1.
CH3-O-CH2-OH
2.
CH2OH-CH2OH
(3)(3分,装置可参考图示1或2,其它如附图的合理答案也得分。进气管和出水管的顺序颠倒扣1分)
 |
|||||
 |
|||||
 |
|||||
图示1 图示2
 |
|||
 |
|||

22、(12分)(1)11.76~11.78均得分 (1分) (2)Na2CO3 和NaHCO3 (1分)因为第一滴定终点所用体积小于第二滴定终点所用体积或V1<(V2-V1)或计算说明 (2分)
(3)以防滴定过快使Na2CO3直接生成H2CO3 (2分)
(4)碱样的总碱量为:
n(Na2O)= [(25.02mL +24.98 mL)/2]×10
(5)直接以溴甲酚绿-二甲基黄或甲基橙为指示剂滴定至终点 (3分)
23、(11分)(1)便于硫被水浸润 (2分)
(2)Na2SO4(1分) 取少量溶液,加稀盐酸酸化后,过滤,再加BaCl2溶液 (2分)
(3)玻璃棒、漏斗、烧杯 (2分);用乙醇或CS2浸没滤渣,等自然流下后,重复几次(2分)。(用水洗涤不得分)
(4)温度应低于
四、(共30分)
24.(11分)(1)NaOH、NaAl(OH)4(NaAlO2)、Na2SiO3 [或氢氧化钠、铝酸钠(偏铝酸钠)、硅酸钠](1分)
(2)CO2+2OH-==HCO3-+2H2O (1分) ,CO2+3H2O+2AlO2-==2Al(OH)3↓+2H2O-+CO32- (1分)
(3) bac (2分) ;
(4)2H2O+2e-→2OH-+H2↑(2分) ;Al(OH)3 +OH-=Al(OH)4- 或Al(OH)3 +OH-=AlO2-+2H2O (2分)
 (5)(2分)
(5)(2分)
25 (8分)
(1)(3分)
V正 < V逆(1分)
0.40(2分)
(2)25%(1分);不变(1分);1:a(1分); (3)-78.7 (2分)
26(11分)(1) (2分)
(2分)
(2)①NH3 或NH4+ (1分);其规律是:硝酸的浓度越大,其还原产物中氮元素化合价越高。(2分)
(其它合理答案均给分。如硝酸的浓度越大,气体生成物中二氧化氮的含量越高;或者,只在硝酸浓度较低时,产物中才会出现氮气。等等)
②B、C、D (对一个或两个给一分,全对2分,但只要出现A、E便不给分) (2分)
③硝酸易挥发,且不稳定,见光易分解,故不易操作;生成物对环境污染严重 (2分)
(3)A.B.D.(2分)(对一个或两个给一分,全对2分,但只要出现C便不给分)
五、(共10分)
27. (共10分) (1)BCD;(共2分,答对两个给1分全对给2分,错选A倒扣1分,答ABCD为0分)
(2)能与羧酸发生酯化反应(或其它合理的答案均可);(2分)
(3)CH3COOH;(2分,写结构式不给分)
(4)AC;(2分,选对一个给一分,错选一个倒扣一分,扣完本小题分为止)
(5)CH2=CH2 + Br2 → CH2Br―CH2Br;(2分,有机物写分子式不给分、写结构式给分,“→”写“=”不给分)
六、选做题(共10分)
28. (共10分)
 |
(1) (2分),取代反应(或酯化反应);(1分)
 |
(2)
(2分,有机物写分子式不给分、写结构式给分,
“→”写“=”扣1分,反应条件错写或漏写扣1分)
(3)b、c、d;(2分,选对两个给1分,选对三个给2分,错选为0分)
 (4)(3分,路线有误或不全者不给分,条件不全或有误者扣一分,其它合理答案酌情给分)
(4)(3分,路线有误或不全者不给分,条件不全或有误者扣一分,其它合理答案酌情给分)
 |
或者
29.(共10分)
(1)LaNi5 + 3H2  LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
(2)CE (2分,每选对一个给一分,每错选一个倒扣一分,扣完本小题分为止)
(3)①[Ar]3d7;或 (2分,写成3d7不给分)
(2分,写成3d7不给分)
②2NiO(OH) + 6HCl(浓)=2NiCl2+Cl2↑+4H2O;(2分,未配平不给分,氯气未写气体符号扣一分)
(4)A和B(或A和C、A和D、B和E、C和E、D和E任一组均可);(2分,若同组中出现同种物质则不给分,例如AE、BC……等)
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com