
题目列表(包括答案和解析)
|
已知:2H2(g)+O2(g)=2H2O(l);ΔH=-571.6 KJ·mol-1 CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890 KJ·mol-1 现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 KJ,则原混合气体中H2与CH4的物质的量之比是 | |
| [ ] | |
A. |
1∶1 |
B. |
1∶3 |
C. |
1∶4 |
D. |
2∶3 |
|
已知 :2H2(g)+O2(g)=2H2O(l);ΔH=-571.6 KJ·mol-1 CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890 KJ·mol-1现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695 KJ,则原混合气体中H2与CH4的物质的量之比是 | |
| [ ] | |
A. |
1∶1 |
B. |
1∶3 |
C. |
1∶4 |
D. |
2∶3 |
下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热
ΔH=2×(-57.3) kJ·mol-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+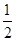 O2(g)=CO2(g)+2H2(g)
ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9
kJ·mol-1
O2(g)=CO2(g)+2H2(g)
ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9
kJ·mol-1
C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g)ΔH=+571.6 kJ·mol-1
D.葡萄糖的燃烧热是2800 kJ·mol-1,则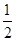 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1
下列关于热化学反应的描述中正确的是( )
| A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热 ΔH=2×(-57.3) kJ·mol-1 |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+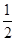 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9 kJ·mol-1 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
| C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g)ΔH=+571.6 kJ·mol-1 |
D.葡萄糖的燃烧热是2800 kJ·mol-1,则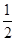 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400 kJ·mol-1 |
|
下列有关热化学方程式的叙述正确的是 | |
| [ ] | |
A. |
已知C(石墨,s) |
B. |
已知C(s)+O2(g)=CO2(g);ΔH1和C(s)+1/2O2(g)=CO(g);ΔH2,则ΔH1>ΔH2 |
C. |
101 KPa时,2 H2(g)+O2(g)=2H2O(l);ΔH=-571.6 kJ·mol-1,则氢气的燃烧热为285.8 kJ·mol-1 |
D. |
含20.0 g NaOH的稀溶液与稀盐酸完全中和时放出28.7 kJ的热量,则该反应的热化学方程式为∶NaOH(aq)+HCl(aq)=NaCI(aq)+H2O(l);ΔH=+57.4 kJ·mol-1 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com