
题目列表(包括答案和解析)
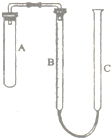 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).| 1 |
| 3 |
| 1 |
| 3 |
 17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).
17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL). 某化学兴趣小组拟用右图装置对某粗锌样品进行纯度检测.按下列实验步骤进行,请填写相关内容.
某化学兴趣小组拟用右图装置对某粗锌样品进行纯度检测.按下列实验步骤进行,请填写相关内容. 我校化学学习兴趣小组同学学习了“用红磷燃烧测定空气中氧气含量”实验之后,认为课本上实验存在不足,实验小组同学在教师的指导下将原装置改进如图所示,成功的测出空气中氧气体积分数.以下是他们的探究过程:
我校化学学习兴趣小组同学学习了“用红磷燃烧测定空气中氧气含量”实验之后,认为课本上实验存在不足,实验小组同学在教师的指导下将原装置改进如图所示,成功的测出空气中氧气体积分数.以下是他们的探究过程:我校化学学习兴趣小组同学学习了“用红磷燃烧测定空气中氧气含量”实验之后,认为课本上实验存在不足,实验小组同学在教师的指导下将原装置改进如图所示,成功的测出空气中氧气体积分数。以下是他们的探究过程:
【查阅资料】白磷的着火点为40℃。
【提出问题】氧气体积约占空气总体积的多少?
【设计实验】①经测定,锥形瓶内空气体积为230mL,则注射器中至少应吸入 mL水(填整数);②检验装置的气密性之后,装入药品,按图所示连接好仪器,夹紧弹簧夹;
③先将锥形瓶底部放入热水中,白磷很快被引燃,然后将锥形瓶从热水中取出;
④待装置冷却后打开弹簧夹。
【实验现象】
白磷燃烧的现象为 ,文字表达式为 ;
气球的变化情况为 。
【实验结论】通过该实验说明空气中氧气的体积分数约为 。
【实验反思】请结合课本装置图分析,该改进装置比课本装置有哪些优点:
① ,② 。
(至少回答两点)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com